
| A. | 离子半径C3->D->B+>A2+ | B. | 原子序数D>C>B>A | ||
| C. | 原子半径A>B>D>C | D. | 单质的还原性A>B>D>C |
分析 短周期元素的离子:A2+,B+,C3-,D-都具有相同的电子层结构,所以A、B在周期表中C、D的下一周期,原子序数:A>B>D>C,结合元素周期律递变规律解答该题.
解答 解:短周期元素的离子:A2+,B+,C3-,D-都具有相同的电子层结构,所以A、B在周期表中C、D的下一周期,原子序数:A>B>D>C.
A.A2+,B+,C3-,D-都具有相同的电子层结构,核电荷数越大,离子半径越小,核电荷数A>B>D>C,所以离子半径C3->D->B+>A2+,故A正确;
B.A2+,B+,C3-,D-都具有相同的电子层结构,所以A、B在周期表中C、D的下一周期,原子序数:A>B>D>C,故B错误;
C.A、B在周期表中C、D的下一周期,原子序数:A>B>D>C,原子核外电子层数越多,半径越大,同周期元素原子序数越大,半径越小,则有原子半径:B>A>C>D,故C错误;
D.A、B在周期表中同周期,原子序数:A>B,金属性:B>A,对应单质的还原性:B>A;而C、D为非金属,单质主要表现氧化性,故D错误;
故选A.
点评 本题考查位置结构性质的相互关系及应用,把握核外电子排布确定元素所在周期表中的位置、元素周期律的递变规律是解答该题的关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
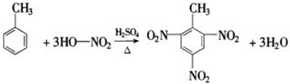

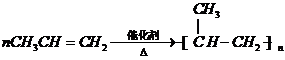
 -CH2CH3+18KMnO4+27H2SO4→5HOOC-
-CH2CH3+18KMnO4+27H2SO4→5HOOC- -COOH+9K2SO4+18MnSO4+5CO2↑+42H2O
-COOH+9K2SO4+18MnSO4+5CO2↑+42H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它的最高价氧化物的水化物是强酸 | B. | 它的金属性比铅强 | ||
| C. | 它具有7个电子层 | D. | 它的最外层电子数为4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu和稀硝酸反应制Cu(NO3)2 | |
| B. | Cu和浓硝酸反应制Cu(NO3)2 | |
| C. | 铜在空气中受热转化为CuO,再溶于稀硝酸制Cu(NO3)2 | |
| D. | 铜在氧气中受热转化为CuO,再溶于浓硝酸制Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
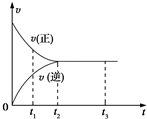 图中是可逆反应X2+3Y2?2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
图中是可逆反应X2+3Y2?2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )| A. | t1时,V(正)>V(逆) | B. | t1~t2,X2的物质的量越来越多 | ||
| C. | t2~t3,各物质的浓度不再发生变化 | D. | t2~t3,反应不再发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



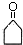 ,G中官能团的名称为酯基、碳碳双键.
,G中官能团的名称为酯基、碳碳双键. +CH3CHO$\stackrel{碱}{→}$
+CH3CHO$\stackrel{碱}{→}$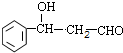 ,反应类型加成反应.
,反应类型加成反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com