
| A. | 9.3 | B. | 9.7 | C. | 10 | D. | 10.7 |
分析 两种碱溶液混合,先计算出混合后溶液中的c(OH-),再根据常温下水的离子积计算出溶液的c(H+),然后根据pH=-lgc(H+)计算混合液的pH.
解答 解:常温下pH=9的NaOH溶液中c(OH-)=1×10-5mol/L,pH=11的NaOH溶液中c(OH-)=1×10-3mol/L,
混合液中氢氧根离子浓度为:c(OH-)=$\frac{1{0}^{-5}+1{0}^{-3}}{2}$mol/L≈$\frac{1{0}^{-3}}{2}$mol/L,
则混合液中的c(H+)=$\frac{{K}_{W}}{c({H}^{+})}$=$\frac{1{0}^{-14}}{\frac{1{0}^{-3}}{2}}$mol/L=2.0×10-11mol/L,
所以混合液的pH=-lg2.0×10-11=11-lg2=10.7,
故选D.
点评 本题考查两种碱溶液混合后的溶液氢离子浓度计算,题目难度不大,明确溶液酸碱性与溶液pH的关系为解答关键,注意先计算溶液中c(OH-),再计算c(H+),试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:多选题
| A. | 若电解熔融MgCl2产生1 mol Mg,理论上转移的电子数约为2×6.02×1023 | |
| B. | 常温下,C(s)+H2O(g)?CO(g)+H2(g) 不能自发进行,则该反应的△H>0 | |
| C. | 石墨能导电,所以石墨属于电解质 | |
| D. | 一定条件下反应2SO2+O2?2SO3达到平衡时,v正(O2)=2v逆(SO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、MnO4-、Na+、Cl- | B. | K+、Mg2+、NO3-、Cl- | ||
| C. | Na+、OH-、NH4+、CO32- | D. | Fe3+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 历史上很多种元素是通过原子光谱发现的 | |
| B. | 鉴别晶体与非晶体,最为科学的方法是X射线衍射法 | |
| C. | 前36号元素中基态电子排布未成对电子数最多的元素,在第四周期第IIIB族 | |
| D. | 金属性越强的金属元素,第一电离能不一定就越小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 科学家根据元素的原子结构和性质,把它们科学有序地排列起来,得到了元素周期表 | |
| B. | 原子序数是按元素原子核电荷数递增的顺序给元素编的号 | |
| C. | 元素周期表上对金属元素、非金属元素用不同的颜色做了区分 | |
| D. | 元素周期表共有7个周期,18个族 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2在葡萄糖中作抗氧化剂 | B. | Fe3O4常用作红色油漆和涂料 | ||
| C. | SiO2可制成太阳能电池 | D. | 漂粉精可用于游泳池的消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
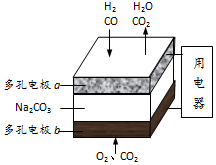
| A. | b是电池的负极 | |
| B. | a电极的反应为:CO+CO32ˉ-2eˉ═2CO2,H2+CO32ˉ-2eˉ═H2O+CO2 | |
| C. | a电极上每消耗22.4L原料气,电池中转移电子数约为2×6.02×1023 | |
| D. | a、b两极消耗的气体的物质的量之比是1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com