
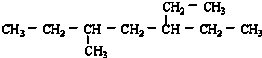
| A. | 4种 | B. | 5种 | C. | 7种 | D. | 8种 |
分析 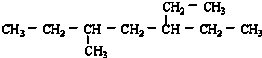 由烯烃和氢气发生加成反应生成,判断碳碳双键的位置可确定烯烃的种类,注意C原子最多形成4个共价键的特点,以此解答该题.
由烯烃和氢气发生加成反应生成,判断碳碳双键的位置可确定烯烃的种类,注意C原子最多形成4个共价键的特点,以此解答该题.
解答 解:根据烯烃与H2加成反应的原理,推知该烷烃分子中相邻碳原子上均含有原子的碳原子间是对应烯烃存在C=C的位置,该烷烃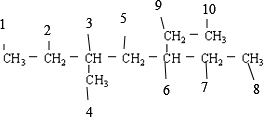 中能形成双键键位置有:1和2之间、2和3之间、3和4之间、3和5之间、5和6之间、6和7之间(6和9)、7和8之间(9和10),故该烯烃共有7种,故选C.
中能形成双键键位置有:1和2之间、2和3之间、3和4之间、3和5之间、5和6之间、6和7之间(6和9)、7和8之间(9和10),故该烯烃共有7种,故选C.
点评 本题考查了加成反应的运用以及同分异构体的书写,为高考常见题型,侧重学生的分析能力的考查,理解加成反应原理是解题的关键,采取逆推法还原C=C双键,注意分析分子结构防止重写、漏写,难度不大.


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+HCl→CH3CH2Cl | B. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | ||
| C. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | D. | 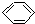 +HO-NO2 $→_{60℃}^{浓硫酸}$ +HO-NO2 $→_{60℃}^{浓硫酸}$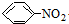 +H2O +H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
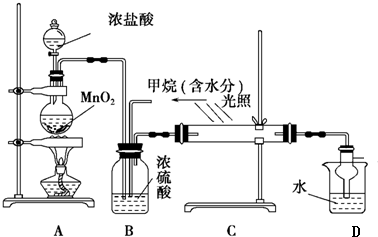
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
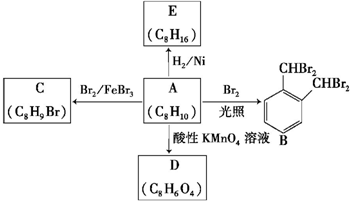 芳香族化合物A是一种基本化工原料,可以从煤和石油中得到.A、B、C、D、E的转化关系如图所示,已知:
芳香族化合物A是一种基本化工原料,可以从煤和石油中得到.A、B、C、D、E的转化关系如图所示,已知: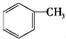 $\stackrel{酸性高锰酸钾}{→}$
$\stackrel{酸性高锰酸钾}{→}$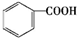
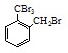 .
.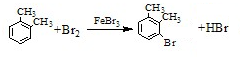 .
.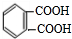 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com