

���� ��1������26��Ԫ�أ���ԭ�Ӻ�����26�����ӣ���ԭ��ʧȥ2�����ӱ��Fe2+�����ݹ���ԭ����дFe2+��������Ų�ʽ��
��2�����ݼ۲���ӶԻ��������ж�Sԭ���ӻ����͡����ӿռ乹�ͣ�ԭ�Ӹ������۵�������ȵ����ǵȵ����壻
��3�����ӷ�����̼̼֮�京��һ���Ҽ�����6����̼��֮�京��һ���Ҽ�����5����̼��֮�京һ���Ҽ�������֮�京һ���Ҽ�������1mol���ӷ����к��ЦҼ�����ĿΪ13mol��
��4�����þ�̯������þ����к��е�ԭ�Ӹ������Ӷ�ȷ���仯ѧʽ��
��� �⣺��1������26��Ԫ�أ���ԭ�Ӻ�����26�����ӣ���ԭ��ʧȥ�����2�����ӱ��Fe2+�����ݹ���ԭ��֪�����̬���Ӻ�������Ų�ʽΪ1s22s22p63s23p63d6 ��[Ar]3d6 ��
�ʴ�Ϊ��1s22s22p63s23p63d6 ��[Ar]3d6 ��
��2��SO2��Sԭ�Ӽ۲���Ӷ�=2+$\frac{1}{2}$��6-2��2��=3�����Բ�ȡsp2�ӻ���ʽ���÷����к���һ���µ��Ӷԣ�������ռ乹����V�Σ�
SO3��ԭ����Ϊ4���۵�����Ϊ24����SO3��Ϊ�ȵ������ΪNO3-��CO32-��BF3��COCl2�ȣ��ʴ�Ϊ��V�Σ�sp2��NO3-��CO32-��BF3��COCl2����
��3�����ӷ�����̼̼֮�京��һ���Ҽ�����6����̼��֮�京��һ���Ҽ�����5����̼��֮�京һ���Ҽ�������֮�京һ���Ҽ�������1mol���ӷ����к��ЦҼ�����ĿΪ13mol��
�ʴ�Ϊ��13 mol����13��6.02��1023����
��4���þ�����Alԭ�Ӹ���Ϊ4��Oԭ�Ӹ���4+4=8��Mgԭ�ӵĸ���Ϊ8��$\frac{1}{8}$+1=2�����Ի�ѧʽΪMgAl2O4���ʴ�Ϊ��MgAl2O4��
���� ���⿼���Ϊ�ۺϣ��漰�����Ų�ʽ���縺�ԡ��ӻ���������Լ�����ṹ������֪ʶ����Ŀ����һ���Ѷȣ�����ע�⾧����ѧʽ�ļ��㷽����


 ��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ᡢ̼�������ֱ�����һԪ�ᡢ��Ԫ�����Ԫ�� | |
| B�� | �����ʵ���Ũ�ȵ�̼����Һ��������Һ��pH��̼����� | |
| C�� | ��̼������Һ��̼��������Һ�ж�������������Ũ�ȹ�ϵ��c��Na+��+c��H+��=c��CO32-��+c��OH-��+c��HCO3-�� | |
| D�� | �����ʵ���Ũ�ȵ�̼������Һ�ʹ�������Һ��pH��̼���ƣ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Һ��������Һ�������� | |
| B�� | ̼��ά����ά�ض����л��߷��� | |
| C�� | �����ͣ�ţ�ͻ�Ϊͬ���칹�� | |
| D�� | ��ͨ������ʯӢ������ˮ�������ǹ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ۡ���ά�غ���֬��������Ȼ�߷��ӻ����� | |
| B�� | ��������Һ�м�������ͭ��Һ���а�ɫ������������ˮ����ɫ���������ܽ� | |
| C�� | ��������CH4��C2H4��C2H2�ֱ�����������ȫȼ�գ����������������μ��� | |
| D�� | ����ʽΪC2H4O2��C4H8O2����������һ������ͬϵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X��Y�γɵĻ�����ֻ��һ�� | |
| B�� | R���⻯������ȶ��Ա�W��ǿ | |
| C�� | ԭ�Ӱ뾶��r��Z����r��R�� | |
| D�� | Y������������ˮ��������Ա�W��ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��Һ��SO42-��Cl-��Mg2+��NH4+ | |
| B�� | ���н϶�Ag+��Һ��SO42-��K+��Na+��OH- | |
| C�� | ��ʹʯ����ֽ���ɫ����Һ��K+��SO32-��NO3-��Na+ | |
| D�� | ���н϶��Al3+����Һ��Na+��SO42-��AlO2-��K+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
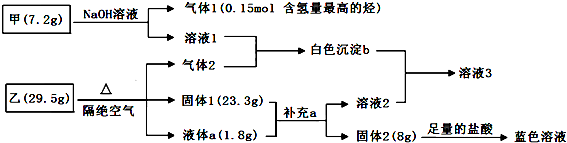
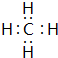 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ����ɫ����Һ��Na+��Mg2+��Cl-��SO42- | |
| B�� | ���ܽ���������ĩ����Һ�У�K+��N03-��Cl-��NH4+ | |
| C�� | �μӱ�����Һ����ɫ����Һ��NH4+��K+��Cl-��H2S | |
| D�� | ��ˮ�������c��H+��=10-12mol��L-1����Һ��Na+��K+��NO3-��C6H5O- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
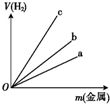 ����һ����Ҫ�ķǽ���Ԫ�أ���ĵ��ʼ��仯�����ڿ�ѧ�о���ҵ���������Ź㷺����Ҫ�����ã�
����һ����Ҫ�ķǽ���Ԫ�أ���ĵ��ʼ��仯�����ڿ�ѧ�о���ҵ���������Ź㷺����Ҫ�����ã�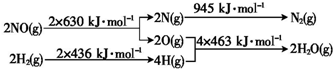
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com