


科目:高中化学 来源: 题型:阅读理解
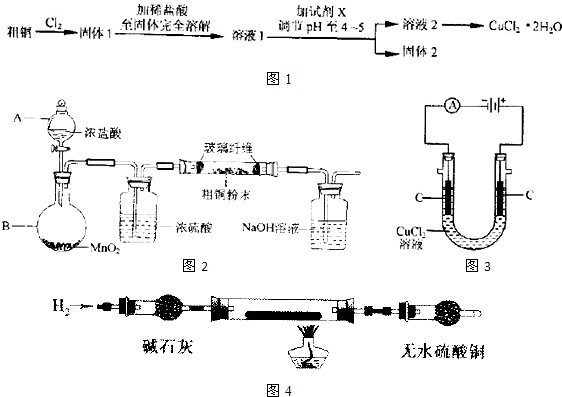
| ||
| ||
| c(CuCl 42- ) |
| c[Cu(H2O) 42- ]?c4(Cl-) |
| c(CuCl 42- ) |
| c[Cu(H2O) 42- ]?c4(Cl-) |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| 8 |
| 3 |
| 8 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
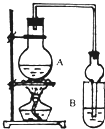 I.下列实验设计、操作或实验现象合理的是
I.下列实验设计、操作或实验现象合理的是| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
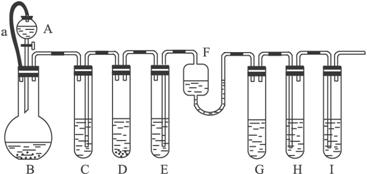
各装置中试剂或物质为:
A:2 mol·L-1 H2SO4 B:Zn C:2 mol·L-1 H2SO4和CuSO4混合液 D:Zn E:CuSO4 F:NH3·H2OG:30% H2O2 H:饱和的H2S溶液 I:NaOH溶液
已知:Cu2++4NH3·H2O====[Cu(NH3)4]2++4H2O,其产物可作H2O2分解的催化剂。
请完成下列问题:
(1)“化学多米诺实验”成功的关键之一是控制好第一个反应,关键之二是____________。
(2)B与D两容器中反应速率比较B______D(填“>”“<”或“=”=,原因是______
_________________________________________________。
(3)H中的现象是________________________________________。
(4)I的作用是(用离子方程式表示)____________________。
(5)A和B之间的导管a的作用是_____________________________。
(6)在该实验中不涉及的反应类型是(填序号)。
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(7)如果从H中导出的气体是极易溶于水的气体,下列哪个装置能代替I?填序号______。
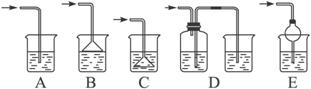
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com