
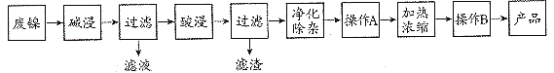
����Ŀ��Ǧ�������Ҫ�ɷ�ΪPbS�������������ַ�����Ǧ������ұ������Ǧ��
I.����Ǧ��Ǧ�����ڿ����б��գ�����PbO��SO2��
(1) ��Ǧ�������Ǧ�ķ�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ_________��
(2) ����Ǧ�ķ����к���Ũ��SO2���ɽ�����ͨ�������ˮ�н��д�������Ӧ�����ӷ���ʽΪ��__________��
II.ʪ����Ǧ���Ʊ�����Ǧ��ͬʱ�������Ƶ���ǣ�����ڻ���Ǧ��Ϊ������ʪ����Ǧ�Ĺ����������£�

��֪��PbCl2��ˮ���ܽ��С����Cl��Ũ�Ƚϴ����Һ�У�����ƽ�⣺PbCl2(s) + 2Cl��(aq)PbCl42��(aq) H��0
(3) ��ȡǦ����ʱ������Ӧ�����ӷ���ʽ��________��
(4) ����Һ1������ PbCl2�IJ���a��_______��
(5) ����Һ3����Һ2�ֱ�������ͼ��ʾ���װ�õ����������У�����ȡ����Ǧ��ʹ��ȡҺ�е�FeCl3������

����Һ3Ӧ����______(������������������������)�С�
�ڼ�����Һ2��������ΪFeCl3�Ŀ���ԭ����_________
����Ǧ���������Ϊa g��Ǧ������Ϊb ����������ͨ��c mol����ʱ������Ǧȫ��������Ǧ������PbS�����������ļ���ʽΪ____________
���𰸡�3:2 SO2+2NH3.H2O= SO32��+2NH4++ H2O PbS+2Fe3++4Cl��= PbCl42��+ 2Fe2++S�� �����¶ȣ���ˮϡ�� ������ ��������Fe2+��2e��= Fe3+�������ҵ�Cl�������ƶ��������ң�ʵ��FeCl3������ ![]()
��������
(1)��Ǧ�ڿ����б�������PbO��SO2����д������ԭ��Ӧ����ʽ��Ȼ����з�����
(2)SO2Ϊ�������壬��ˮ�Լ��ԣ���Ӧ����(NH4)2SO3��
(3)�������̣�PbS��Sת����S���ʣ�������Fe3���������ԣ�������Ϣ����д�����ӷ���ʽ��
(4)PbCl2��ˮ���ܽ��С����Cl��Ũ�Ƚϴ����Һ�У����ڣ�PbCl2(s) + 2Cl��(aq)PbCl42��(aq) H��0�����PbCl2����ƽ�����淴Ӧ������У�
(5)�ٸ������̻��Pb��PbԪ�صĻ��ϼ۽��ͣ����ݵ��ԭ����Ӧ����Һ3���������ң�
�ڸ������̣���Һ2�к���Fe2�������FeCl3�����ϼ����ߣ���Ҫ����Һ2���������ң�
�۸���PbԪ���غ���з����ͼ��㣻
(1)��Ӧ����ʽΪ2PbS + 3O2= 2PbO+2SO2��SԪ�صĻ��ϼ����ߣ�PbԪ�صĻ��ϼ۲��䣬��PbSΪ��ԭ��������Ϊ���������������뻹ԭ�������ʵ���֮��Ϊ3:2��
�𰸣�3��2��
(2)���ڰ�ˮ��������Ӧ�������Σ����ӷ���ʽΪ��SO2+2NH3.H2O= SO32��+2NH4++ H2O��
�𰸣�SO2+2NH3.H2O= SO32��+2NH4++ H2O��
(3)�������̣�����1�к������ʣ�˵��PbS�е�SԪ��ת����S���ʣ����ϼ����ߣ�Fe3������������������Ϣ��PbԪ����PbCl42������˽�ȡ�������ӷ���ʽΪPbS+2Fe3++4Cl��= PbCl42��+ 2Fe2++S����
�𰸣�PbS+2Fe3++4Cl��= PbCl42��+ 2Fe2++S����
(4)��Һ1��ǦԪ�ش��ڵ���ʽΪPbCl42��������PbCl2(s) + 2Cl��(aq) ![]() PbCl42��(aq) H��0�������¶Ⱥͼ�ˮϡ��������ƽ�������ƶ���
PbCl42��(aq) H��0�������¶Ⱥͼ�ˮϡ��������ƽ�������ƶ���
��Ϊ�����¶ȣ���ˮϡ�ͣ�
(5)����Һ3����Һ2�е����ʷֱ���PbCl42����FeCl2�������Ҫʵ��FeCl2ת��ΪFeCl3������������Ӧ������Һ2���������ң�PbCl42��ת��ΪPb��������ԭ��Ӧ����Һ3���������ң�
�𰸣������ң�
�ڸ��ݢٷ��������FeCl3��������������Fe2+��2e��= Fe3+�������ҵ�Cl�������ƶ��������ң�ʵ��FeCl3��������
�𰸣���������Fe2+��2e��= Fe3+�������ҵ�Cl�������ƶ��������ң�ʵ��FeCl3��������
����Ǧ������PbS����������Ϊx��PbCl42�����2mole������Pb��������ͨcmol����ʱ�����n(Pb)=![]() mol������ǦԪ���غ㣬�ó�
mol������ǦԪ���غ㣬�ó�![]() =
=![]() mol�������PbS����������Ϊ
mol�������PbS����������Ϊ![]() ��
��
�𰸣�![]() ��
��


 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д� ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W���ֶ�����Ԫ�ص�ԭ��������������ԭ������������֮��Ϊ13��X��ԭ�Ӱ뾶��Y��С��X��Wͬ���壬Z��������������������3��������˵������ȷ����
A.����Ԫ�ؼ����ӵİ뾶��X<Y<Z<W
B.X��Y�γɵ����ӻ������мȺ����Ӽ��ֺ����ۼ�
C.���ӻ�����W2Z2������������֮��Ϊ1:1
D.ֻ��X��Y��Z����Ԫ�صĻ�����һ���ǹ��ۻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭпԭ��أ���ͼ������ʱ����������������ǣ� ��

A. ������ӦΪ��Cu2++2e�C= Cu
B. ��ط�ӦΪ��Zn+Cu2+=Zn2+ +Cu
C. �����·�У����ӴӸ�����������
D. �����е�K+����ZnSO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��H2(g)��![]() O2(g)=H2O(g) ��H1
O2(g)=H2O(g) ��H1
![]() N2(g)��O2(g)=NO2(g) ��H2
N2(g)��O2(g)=NO2(g) ��H2
![]() N2(g)��3/2H2(g)=NH3(g) ��H3
N2(g)��3/2H2(g)=NH3(g) ��H3
��Ӧ2NH3(g)��![]() O2(g)=2NO2(g)��3H2O(g)����HΪ�� ��
O2(g)=2NO2(g)��3H2O(g)����H�� ��
A. 2��H1��2��H2��2��H3B. ��H1����H2����H3
C. 3��H1��2��H2��2��H3D. 3��H1��2��H2��2��H3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ҫ��Ni������Al��Fe��SiO2�������������ᡢ������ʡ����÷��������Ʊ�NiSO4��7H2O���壬��������ͼ��
��֪��Ksp[Fe(OH)3]=8.0��10��38��Ksp[Fe(OH)2]=8.0��10��16��Ksp[Al(OH)3]=3.2��10��34��Ksp[Ni(OH)2]=2.0��10��15��1g2=0.3��
�ش���������
��1�������ʱ���������ӷ���ʽΪFe+2H+=Fe2++H2����____��
��2��������������Ҫ�ȼ���H2O2��Һ��������Ӧ�����ӷ���ʽΪ___��
��3��Ni2+��ǿ������Һ�л��ɱ�NaClO����ΪNiOOH���÷�Ӧ���ӷ���ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ը�����(��Ҫ�ɷ�ΪFeO��Cr2O3��������Al2O3������)Ϊԭ���Ʊ��������Ĺ���������ͼ��ʾ��

��1���������������ù���ΪNa2CrO4��Fe2O3��NaAlO2��
����������ʱFeO��Cr2O3������Ӧ�Ļ�ѧ����ʽΪ____��
����������ʱAl2O3������Ӧ�Ļ�ѧ����ʽΪ____��
��2������pH=7��ʱ����Al(OH)3�����ӷ���ʽΪ____��
��3������������������ΪCr(OH)3������ԭ����Ӧ�����ӷ���ʽΪ____��
��4����ұ����ʱ�Ļ�ѧ����ʽΪ____��
��5������������Է�ˮ����ͼ2��ʾ����������д�������ĵ缫��Ӧʽ��____��
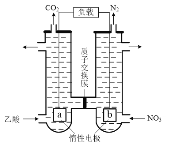
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����⻯��(NaBH4)��������ԭ�������Ϸ��ݼ������ڴ�����������ˮ��Ӧ��ȡ�������۹�����ͼ��ʾ������˵������ȷ����
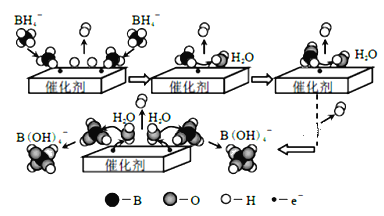
A.NaBH4����Ԫ�صĻ��ϼ�Ϊ+1��
B.����D2O����H2O����Ӧ�����ɵ������к���H2��HD��D2
C.ͨ�����ƴ����������ͱ���������Կ��������IJ�������
D.NaBH4 ��ˮ��Ӧ�����ӷ���ʽΪ��BH4��+4H2O=B(OH)4��+4H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1200 ��ʱ����Ȼ���������лᷢ�����з�Ӧ��H2S(g)��![]() O2(g)= SO2(g)��H2O(g)����H1��H2S(g)��
O2(g)= SO2(g)��H2O(g)����H1��H2S(g)��![]() O2(g)= S(g)��H2O(g)����H2��2H2S(g)��SO2(g)=
O2(g)= S(g)��H2O(g)����H2��2H2S(g)��SO2(g)= ![]() S2(g)��2H2O(g)����H3��2S(g)= S2(g)����H4 ����H4����ȷ����ʽΪ�� ��
S2(g)��2H2O(g)����H3��2S(g)= S2(g)����H4 ����H4����ȷ����ʽΪ�� ��
A.��H4��![]() (��H1����H3��3��H2)B.��H4��
(��H1����H3��3��H2)B.��H4��![]() (3��H2����H1����H3)
(3��H2����H1����H3)
C.��H4��![]() (��H1����H3��3��H2)D.��H4��
(��H1����H3��3��H2)D.��H4��![]() (��H1����H3��3��H2)
(��H1����H3��3��H2)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɺ����ˮ��ȡ����ص�һ�ֹ������£�

����KI(aq)��ʱ�����¶���ˮ�����ӻ�ΪKw��1.0��10��13��Ksp[Fe(OH)2]��9.0��10��15��Ϊ����0.9 mol��L��1 FeI2��Һ��Fe2+ˮ�����ɽ�״������I-����ʼ����K2CO3���뱣����Һ��pH������______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com