
【题目】(1)等质量的CO和SO2分别装入同温同体积的容器,所含分子数之比 ,所含氧原子之比 ,密度之比 ,压强之比 。
(2)将标准状况下224L的HCl溶于1000g水配成密度为1.23g/cm3溶液,所得溶液的物质的量浓度为________。
【答案】(1)16:7 8:7 1:1 16:7 (2)9mol/L
【解析】
试题分析:
(1)根据n=![]() 可知,等质量的CO和SO2,它们的物质的量之比等于摩尔质量的反比,即:64g/mol:28g/mol=16:7;根据N=nNA可知,CO和SO2所含分子数目之比等于CO和SO2物质的量之比=16:7;CO和SO2中所含氧原子数目之比=(16×1):(7×2)=8:7;根据ρ=
可知,等质量的CO和SO2,它们的物质的量之比等于摩尔质量的反比,即:64g/mol:28g/mol=16:7;根据N=nNA可知,CO和SO2所含分子数目之比等于CO和SO2物质的量之比=16:7;CO和SO2中所含氧原子数目之比=(16×1):(7×2)=8:7;根据ρ=![]() 可知,质量相等体积也相等,故密度也相等,即密度之比为1:1;由PV=nRT可推出PV=
可知,质量相等体积也相等,故密度也相等,即密度之比为1:1;由PV=nRT可推出PV=![]() RT,当等质量的CO和SO2分别装入同温同体积的容器,则压强之比等于摩尔质量的反比=16:7;
RT,当等质量的CO和SO2分别装入同温同体积的容器,则压强之比等于摩尔质量的反比=16:7;
(2)氯化氢的物质的量n=![]() =
= ![]() =10mol;氯化氢的质量m=nM=10mol×36.5g/mol=365g;溶液的体积V=
=10mol;氯化氢的质量m=nM=10mol×36.5g/mol=365g;溶液的体积V= ![]() =
=![]() ;c=
;c= ![]() =9mol/L 。
=9mol/L 。


科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G、H、I九种物质,其中A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G、F是单质,其余均为化合物,H是一种淡黄色固体,它们的转化关系如图所示。请回答:

(1)画出G离子结构示意图________;
(2)写出B、I的化学式B________,I________;
(3)写出H的一种用途__________________________________;
(4)写出A受热分解的化学方程式_________________________;
(5)若H与C反应固体增重4.2 g,则参加反应的C气体在标准状况下的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸锰(MnCO3)是理想的高性能强磁性材料,也是制备Mn2O3、MnO2等锰的氧化物的重要原料,广泛用于电子、化工、医药等行业。
(1)工业上制备方程式为:MnSO4+2NH4HCO3=MnCO3↓+(NH4)2SO4+CO2↑+H2O。反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4.加入稍过量的NH4HCO3的目的是 。
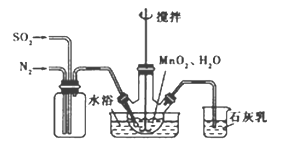
(2)实验室模拟工业二氧化锰制备硫酸锰装置如图
①石灰乳参与反应的化学方程式为 。
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有 。
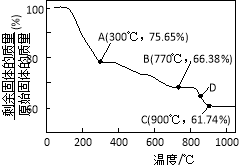
(3)MnCO3在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温度的变化如图所示。则300℃时,剩余固体中n(Mn)∶n(O)为 ;图中点D对应固体的成分为 (填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所含分子数由多到少的排列顺序是 (用字母排序)
A.标准状况下33.6LH2
B.所含电子的物质的量为4mol的H2
C.20℃时45gH2O
D.常温下,16gO2与14gN2的混合气体
E.含原子总数约为1.204×1024的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化。实验时必须使用铁屑和6 mol/L的稀硫酸,其他试剂任选。

请回答下列问题:
(1)B装置中盛有一定量的NaOH溶液,A装置中应预先加入的试剂是________,A装置中发生反应的离子方程式是___________。
(2)实验开始时应先将活塞a________(填“打开”或“关闭”)。
(3)简述制取Fe(OH)2的操作过程__________________。
(4)实验完毕,拔去B装置中的橡胶塞,放入一部分空气,此时B装置中发生反应的化学方程式为_______________________。
(5)在下图中,装置________(填序号)能较长时间观察到Fe(OH)2白色沉淀。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液。
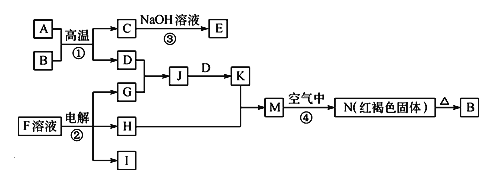
请回答下列问题:
(1)B的化学式为 。
(2)H的电子式为 。
(3)写出反应②的离子方程式 。
(4)写出反应④的化学方程式 。
(5)D是目前应用最广泛的金属,D与炭混合物在水溶液中可形成许多微电池。将含有Cr2O72–的酸性废水通过该混合物,在微电池 极上Cr2O72–转化为Cr3+,其电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫的化合物再生产和生活中有广泛的应用,其吸收和处理及相互转化具有广泛的意义
(1)二氧化硫具有还原性,可以和许多氧化剂反应,二氧化硫气体通入硫酸酸化的重铬酸钾溶液中,恰好生成铬钾钒[ KCr(SO4)2.12H2O],写出反应的化学方程式反应中被还原的元素
(2)过量二氧化硫通入硫化钠溶液可以看到黄色沉淀,产物还有一种盐,写出反应的离子方程式
(3)在1L0.3mol/L的氢氧化钠溶液中,通入4.48L二氧化硫(标况)反应后得到的溶液中微粒的浓度之间有一些等量关系: 任写一个
(4)燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关键。SO2烟气脱除的一种工业流程如下:
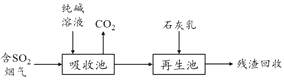
① 用纯碱溶液吸收SO2将其转化为HSO3-,反应的离子方程式是 。
② 若石灰乳过量,将其产物再排回吸收池,其中可用于吸收SO2的物质的化学式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com