
�����ʵ�顱���м��ס����㡢��Լ����ɫ���ŵ㣬�۲������ĸ������ʵ�顱���г�װ��δ���������ж�����˵����ȷ���ǣ�������
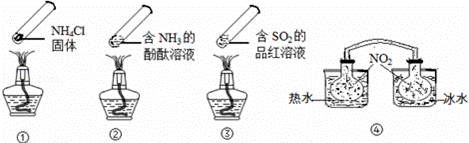
| �� | A�� | ����ʱ�����ϲ��㼯�˹���NH4Cl��˵��NH4Cl�����ȶ��ԱȽϺ� |
| �� | B�� | ����ʱ���ڡ�����Һ����죬��ȴ���ֶ���Ϊ��ɫ |
| �� | C�� | ���У���������ˮ�е�������������ɫ��������ڱ�ˮ�е�������������ɫ��dz |
| �� | D�� | �ĸ������ʵ�顱���������Ļ�ѧ��Ӧ���ǿ��淴Ӧ |
| ����ʵ�鷽������ƣ� | |
| ר�⣺ | Ԫ�ؼ��仯�����ѧʵ����������� |
| ������ | A���Ȼ�立ֽ����ɰ������Ȼ��⣬�Ȼ���Ͱ�����Ӧ�����Ȼ�泥� B�����ݰ���ʹ��̪����ԭ����𣬸��ݶ���������Ʒ�����õ�ԭ����� C�����ݶ��������Ŀ��淴Ӧ�ͻ�ѧƽ���ԭ����� D�����淴Ӧ������ͬ�������£�����������Ӧ���У��������淴Ӧ���У� |
| ��� | �⣺A������ʱ�����ϲ��㼯�˹���NH4Cl�������ڼ���ʱ�Ȼ�立ֽ����ɰ������Ȼ��⣬�������Ȼ������ԹܵĶ�����Ӧ�����Ȼ�泥�����NH4Cl�����ȶ��ԱȽϺã���A���� B�����а�ˮ�Լ��ԣ�ʹ��̪��죬����ʱ�������ݳ�����ȴ�����ֺ�ˮ��Ӧ����ɺ�ɫ������������Ʒ������ɫ�����Ⱥ���������ݳ����Ժ�ɫ����B���� C��2NO2 ��g��⇌N2O4��g����H=��92.4kJ/mol������ӦΪ���ȷ�Ӧ�������¶�ƽ�����淴Ӧ�����ƶ�������ɫ������н�������ˮ�е�������������ɫ�����֮��dz�����Խ����ڱ�ˮ�е�������������ɫ��dz����C��ȷ�� D���Ȼ�����ȷֽ⣬�백�����Ȼ��ⷴӦ�����Ȼ�鱗��ǿ��淴Ӧ����ǰ������ȣ�����ֻҪ�ڳ����£���D���� ��ѡ��C�� |
| ������ | �����ԡ����ʵ�顱Ϊ���壬��������صķ�Ӧ����������������صĻ�ѧ��Ӧ����ʽ����Ŀ�ϼ� |
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Ҵ������ͺͱ��ӵĹ�ͬ����(����)
A�����ӽṹ�ж������� ����������Na��Ӧ������H2
����������Na��Ӧ������H2
B��������NaOH��Һ�����кͷ�Ӧ
C����FeCl3��Һ��Ӧ����ɫ
D�������¶�����ɫҺ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��Һ��Al��Ӧ�ܷų�H2�����������ڸ���Һ��һ���ܴ����������
A��NH4����Fe2����NO3����SO42�� B��Na����K����Cl����SO42��
C��Mg2����H����Cl����NO3�� D��K����Ca2����HCO3����Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NAΪ����٤��������ֵ������������ȷ���ǣ�������
| �� | A�� | ���³�ѹ�£�23g��NO2���е���ԭ����ΪNA |
| �� | B�� | ��֪ij��Ԫ�ص�һ��ԭ�ӵ�����Ϊag�����Ԫ�ص����ԭ����������ΪaNA |
| �� | C�� | ij�ܱ�����ʢ��0.1molN2��0.4molH2����һ�������³�ַ�Ӧ��ת�Ƶ��ӵ���ĿΪ0.6NA |
| �� | D�� | 80gNH4NO3�������NH4+��NA�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ������Fe��FeO��Fe3O4��Fe2O3�Ļ�����м���250mL 4mol/L��ϡ���ᣬǡ��ʹ�������ȫ�ܽ⣮�ų�2.24L NO����״��������������Һ�м���KSCN��Һ����Ѫ��ɫ���֣����������������ڼ����»�ԭ��ͬ�����Ļ����ܵõ��������ʵ���Ϊ��������
| �� | A�� | 0.21mol | B�� | 0.25mol | C�� | 0.45mol | D�� | 0.5mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ����MgCl2��AlCl3�����Һ�У��Ⱥ�����Լ�A��Bʱ���ó������ʵ���y��mol�� ���Լ����V��mL����Ĺ�ϵͼ����ʼ�μ�6mL�Լ�A������μ�A���ɣ�֮��ĵ��Լ�B�����½�����ȷ���ǣ�������
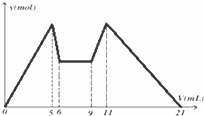
| �� | A�� | ������NaOH��B���������ᣬ��2C��A��=C��B�� |
| �� | B�� | ��A��B��ΪһԪǿ���һԪǿ���μ�7mL�Լ�A��ĵ��Լ�B |
| �� | C�� | A������Ba��OH��2��B���������ᣬ��C��A��=C��B�� |
| �� | D�� | ԭ���Һ�У�c��Al3+����c��Mg2+����c��Cl����=1��2��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ö������ȡ������ƣ�Na2FeO4�������;�ˮ�������ͳ�ľ�ˮ��Cl2�Ե�ˮ���������dz�������ˮ�����¼�����ClO2��Na2FeO4��ˮ���������зֱ𱻻�ԭΪCl����Fe3+��
��1������Ե�λ���������������õ��ĵ���������ʾ����Ч�ʣ���ô��ClO2��Na2FeO4��Cl2��������ɱ����������Ч���ɴ�С��˳��������������������
��2��Na2FeO4����ˮ��ų�һ����ɫ��ζ���壬��ɱ������������ˮ�е��������ʵ�ԭ���������ӷ���ʽ��ʾΪ����
��3����ҵ��CH3OH��NaClO3Ϊԭ����������������ȡClO2��ͬʱ����CO2���壬��֪�÷�Ӧ��Ϊ�������У���һ��Ϊ2ClO3��+2Cl��+4H+=2ClO2��+Cl2��+2H2O
��д���ڶ�����Ӧ�����ӷ���ʽ��
�ڹ�ҵ����ʱ���ڷ�Ӧ���м�����Cl����������������
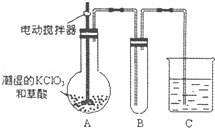
��4����֪����������һ�ֻ���ɫ�д̼�����ζ�����壬���۵�Ϊ��59�棬�е�Ϊ11.0�棬������ˮ����ҵ�����Գ�ʪ��KClO3�Ͳ�����60��ʱ��Ӧ�Ƶã�ClO2Ҳ���Կ����������ᣨHClO2�������ᣨHClO3���Ļ��������ijѧ������ͼ��ʾ��װ��ģ�ҵ��ȡ���ռ�ClO2������AΪClO2�ķ���װ�ã�BΪClO2������װ�ã�CΪβ������װ�ã����ʣ�
��A���ֻ�Ӧ�����¶ȿ��ƣ���ˮԡ���ȣ�װ�ã�B���ֻ�Ӧ����ʲôװ����
��C��Ӧװ���Լ�Ϊ���� C�з�����Ӧ�Ļ�ѧ����ʽΪ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ϊ��֤�����ԣ�Cl2>Fe3+>SO2��ij
С������ͼ��ʾװ�ý���ʵ�飨�г������ͼ��м���װ�����ԣ��������Ѽ��飩��
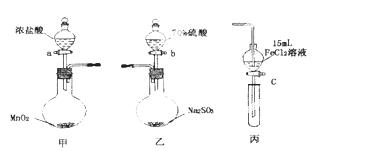
ʵ�鲽�裺
���ڼ�װ���У�����a�����ȣ���װ���г�������ɫ����ʱ�����װ�����ӡ�
�ڵ���װ����FeC12��Һ���ʱ��ֹͣ���ȡ�
�۴���c��ʹԼ2mL����Һ�����Թ��У�������Һ�е����ӡ�
������װ���У�����b���������ž������в���������ͨ��������װ�ñ�ƺ����Һ�У�һ��ʱ���ֹͣ��
�ݸ��±����Թܣ�����c��ʹԼ2mL����Һ�����Թ��У�������Һ�е����ӡ�
�ش��������⣺
��1�����з�����Ӧ�Ļ�ѧ����ʽΪ___________________________________________��
��2����70%��������ȡSO2����Ӧ���ʱ���98%������죬ԭ����__________________��
��3��ʵ���У�֤��������Fe3+��SO2�����ӷ���ʽΪ_____________________________��
��4����I��II��III����ͬѧ�ֱ����������ʵ�飬ʵ�������£�
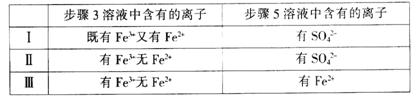
����ʵ����һ���ܹ�֤��������:Cl2>Fe3+>SO2����___________���á�I������II������III�����Żش𣩡�
��5����Ҫ�����ϼͱ�װ��֤��������Ϊ��Cl2> Fe3+> I2�Ľ��ۣ�����Ϊ��
��������©���м��������Լ�_________��_________��һ���ܼ�__________��
�ڽ���װ���в�����Cl2����ͨ����У��۲����©������Һ��ɫ�仯��
������۲쵽������Һ_______________________________________�������ȷ��
��ֹͣͨ��Cl2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����SO2�������Ƿ���CO2����Ӧ�õķ�����
A��ͨ��ʯ��ˮ B����ͨ������KMnO4��Һ��ͨ��ʯ��ˮ
C��ͨ��Ʒ����Һ D����ͨ��С�մ���Һ��ͨ��ʯ��ˮ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com