
| A. | 二氧化硫具有还原性,能与强氧化性的高锰酸钾发生氧化还原反应 | |
| B. | 因为二氧化硫具有漂白性,能使品红溶液永久褪色 | |
| C. | 大气中二氧化碳浓度高时能形成酸雨 | |
| D. | 浓硫酸常用作干燥剂,因为浓硫酸具有脱水性 |
分析 A.二氧化硫中硫元素为+4价,具有强的还原性;
B.二氧化硫的漂白性具有暂时性特点;
C.二氧化硫、氮氧化物是形成酸雨的成分;
D.浓硫酸常用作干燥剂是因为浓硫酸具有吸水性.
解答 解:A.二氧化硫具有还原性,能与强氧化性的高锰酸钾发生氧化还原反应,故A正确;
B.二氧化硫的漂白性具有暂时性特点,加热会导致恢复原色,故B错误;
C.二氧化硫、氮氧化物是形成酸雨的成分,二氧化碳是造成温室效应的气体,故C错误;
D.浓硫酸常用作干燥剂是因为浓硫酸具有吸水性,故D错误;
故选:A.
点评 本题考查二氧化硫的还原性、漂白性及污染和浓硫酸的性质,熟悉物质的性质是解题关键,注意二氧化硫漂白性的特点,题目难度不大.


科目:高中化学 来源: 题型:解答题
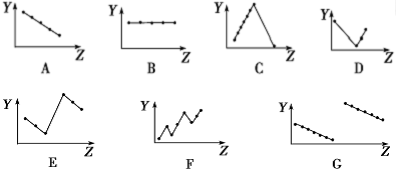
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
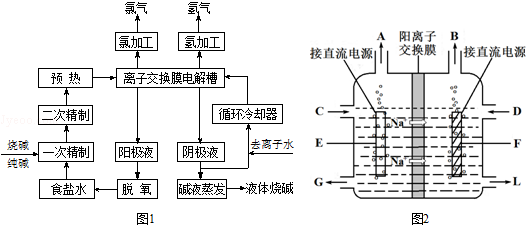
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子晶体中共价键越强,熔点越高 | |
| B. | 原子晶体中分子间作用力越强,熔点越高 | |
| C. | 氯化钠晶体熔化时离子键发生断裂 | |
| D. | 金属晶体熔化时金属键未发生断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,Zn为负极,负极区PH变大 | |
| B. | 电池负极的电极反应式为:2MnO2(s)+H2O(l)+2e-═Mn2O3(s)+2OH-(aq) | |
| C. | 电池工作时,电子由正极流向负极 | |
| D. | 电解质氢氧化钾溶液中阳离子迁移到电池的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2是氧化剂,KOH是还原剂 | |
| B. | 有3molCl2参加反应,就有6NA个电子转移 | |
| C. | 被还原的氯原子和被氧化的氯原子的个数比是1:1 | |
| D. | 被还原的氯原子和被氧化的氯原子的个数比是5:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
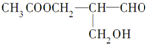 )有光学活性.则该有机化合物分别发生如下反应后,生成的有机物仍有光学活性的是( )
)有光学活性.则该有机化合物分别发生如下反应后,生成的有机物仍有光学活性的是( )| A. | 与乙酸发生酯化反应 | B. | 与NaOH水溶液共热 | ||
| C. | 与银氨溶液作用 | D. | 在催化剂存在下与氢气作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
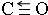 .NH3分子中N原子的杂化方式为SP3杂化,NH3分子的空间立体构型是三角锥型.
.NH3分子中N原子的杂化方式为SP3杂化,NH3分子的空间立体构型是三角锥型.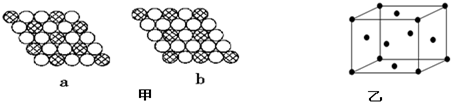
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com