
某些化学键的键能数据如下表所示(kJ·mol-1):
|
键 |
H-H |
Br-Br |
I-I |
Cl-Cl |
H-Cl |
H-I[ |
H-Br |
|
键能 |
436 |
193 |
151 |
247 |
431 |
299 |
356 |
分析上表中数据,下列结论正确的是
A.把1mol Cl2分解为气态原子时,需要放出247 kJ能量
B.由表中所列化学键形成的单质分子中,最稳定的是H2 ,形成的化合物分子中,最不稳定的是HI
C.在一定条件下,1mol H2 与足量的Cl2 、Br2 、I2 分别反应,放出热量由多到少的是I2 > Br2 > Cl2
D.预测1mol H2 在足量F2 中燃烧比在Cl2中放热少
科目:高中化学 来源: 题型:
| 常温 |
| 1 |
| 2 |
| 1 |
| 2 |
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ?mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| 3 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 化学键 | C-C | C-H | H-H | C-O | C≡O(CO) | H-O |
| 键能/kJ?mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| 1 |
| 2 |
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ?mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| 3 |
| 2 |
| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
| 3 |
| 2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | N≡N | H-H | N-H |
| 键能kJ?mol-1 | 946 | 436 | 390 |

查看答案和解析>>
科目:高中化学 来源:2013届浙江省温州市十校联合体高三上学期期初考试化学试卷(带解析) 题型:填空题
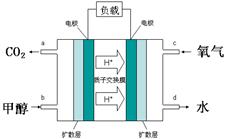
(12分)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合制备甲醇,该反应的热化学方程式为:CO(g)+2H2(g) CH3OH(g) ⊿H 已知某些化学键的键能数据如下表:
CH3OH(g) ⊿H 已知某些化学键的键能数据如下表:
| 化学键 | C—C | C—H | H—H | C—O | C≡O | H—O |
| 键能/kJ·mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com