
氮化硅是一种新合成的结构材料,它是一种超硬、耐磨、耐高温的物质。下列各组物质熔化时,所克服的粒子间作用力与氮化硅熔化时所克服的作用力相同的是( )
A.NaNO3和金刚石 B.晶体硅和石英
C.Cu和MgCl2 D.蔗糖和碘
科目:高中化学 来源: 题型:
利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55 mol·L-1 NaOH溶液,并用另一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均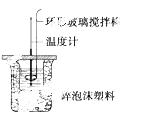 匀,测得混合液最高温度
匀,测得混合液最高温度 。回答下列问题:
。回答下列问题:
(1)为什么所用NaOH溶液要稍过量?__________________
________________________________________________________。
(2)倒入NaOH溶液的正确操作是__________(填序号)。
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是________(填序号)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol·L-1的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为________________。
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为 了计算中和热,某学生实验记录数据如下:
了计算中和热,某学生实验记录数据如下:
| 实验序号 |
| 终止温度t2/ ℃ | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=__________(结果保留一位小数)。
(6)________(填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质在固态时分类中正确的一组是( )
| 选项 | 离子晶体 | 原子晶体 | 分子晶体 |
| A | KOH | Ne | SO2 |
| B | H2SO4 | Fe | S |
| C | CH3COONa | 水晶 | 白磷 |
| D | Ba(OH)2 | 金刚石 | 玻璃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于蛋白质的叙述正确的是( )
A.蛋白质均为天然高分子化合物
B.蛋白质均溶于水,加热能使其变性
C.蛋白质水解的最终产物是氨基酸
D.在蛋白质溶液中加入饱和硫酸铵溶液,析出的蛋白质的生理功能发生了改变
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某蛋白质含N的质量分数为15%,若成年人每天排出尿素25 g,则他每天从食物中摄取的蛋白质的质量平均为( )
A.77.8 g B.66.9 g
C.90.7 g D.106 g
查看答案和解析>>
科目:高中化学 来源: 题型:
有NO、CO2、N2O4三种气体,它们分别都含有0.5 mol氧原子,则三种气体的物质的量之比为( )
A.1:2:4 B.1:1:1
C.4:2:1 D.1:2:4
查看答案和解析>>
科目:高中化学 来源: 题型:
20世纪90年代初,国际上提出了“预防污染”这一新概念。绿色化学是“预防污染”的根本手段,它的目
标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各个环节中都实现净化和
无污染。
(1)下列各项属于“绿色化学”要求的是________。
A.处理废弃物 B.治理污染点
C.减少有毒物 D.杜绝污染源
(2)在我国西部大开发中,某省为筹建一大型化工基地,征集到下列方案,其中你认为可行的是____。
A.建在西部干旱区可以脱贫致富
B.应建在水资源丰富和交通方便且远离城市的郊区
C.企业有权自主选 择厂址
择厂址
D.不宜建在人口稠密的居民区
(3)某化工厂排放的污水中含有Mg2+、Fe3+、C u2+、Hg2+四种离子。甲、乙、丙三位学生分别设计了从该污水中回收纯净的金属铜的方案。
u2+、Hg2+四种离子。甲、乙、丙三位学生分别设计了从该污水中回收纯净的金属铜的方案。
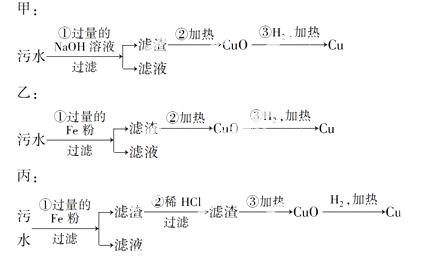
在能制得纯铜的方案中,哪一步操作会导致环境污染?________________。应增加哪些措施防止污染?____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com