
【题目】有Ⅰ、Ⅱ、Ⅲ3个体积均为0.5L的恒容密闭容器,在Ⅰ、Ⅱ、Ⅲ中按不同投料比(Z)充入HCl和O2(如下表),加入催化剂发生反应:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)△H。HCl的平衡转化率与Z和T的关系如图所示。
2Cl2(g)+2H2O(g)△H。HCl的平衡转化率与Z和T的关系如图所示。
容器 | 起始时 | ||
T/℃ | n(HCl)/mol | Z | |
Ⅰ | 300 | 0.25 | a |
Ⅱ | 300 | 0.25 | b |
Ⅲ | 300 | 0.25 | 4 |
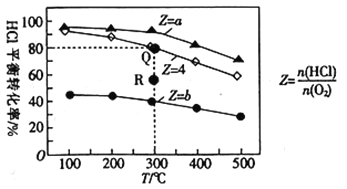
下列说法不正确的是( )
A. △H<0
B. a<4<b
C. 若容器Ⅲ反应某时刻处于R点,则R点的反应速率:v(正)>v(逆)
D. 300℃时,该反应平衡常数的值为320
【答案】D
【解析】A、由图象可知,随着温度的升高HCl的平衡转化率在减小,即升温平衡向左移动,则该反应是放热反应,△H<0,所以A正确;B、在相同温度时,n(HCl)相同,Z=a时HCl的转化率大于Z=4时HCl的转化率,即Ⅰ容器中增大了n(O2),使Z<4,即a<4,同理可得4<b,所以B正确;C、容器Ⅲ 即Z=4时,反应某时刻处于R点,即HCl的转化率小于平衡时HCl的转化率,则反应向正向进行,即v(正)>v(逆),所以C正确;D、由于平衡常数K只与温度有关,因此可根据容器Ⅲ对应的Q点进行计算,4HCl(g)+O2(g)![]() 2Cl2(g)+ 2H2O(g)平衡时HCl的转化率为80%,则起始时c(HCl)=0.5mol/L,由Z=4求得c(O2)= 0.125mol/L,而c(Cl2) =c(H2O)=0,平衡时c(HCl)=0.1mol/L ,c(O2)=0.025mol/L,c(Cl2) =c(H2O)=0.2 mol/L,则K=
2Cl2(g)+ 2H2O(g)平衡时HCl的转化率为80%,则起始时c(HCl)=0.5mol/L,由Z=4求得c(O2)= 0.125mol/L,而c(Cl2) =c(H2O)=0,平衡时c(HCl)=0.1mol/L ,c(O2)=0.025mol/L,c(Cl2) =c(H2O)=0.2 mol/L,则K=![]() =640 (mol/L)-1,所以D错误。本题正确答案为D。
=640 (mol/L)-1,所以D错误。本题正确答案为D。


科目:高中化学 来源: 题型:
【题目】B、C、N、O、Si、S 是几种常见的重要非金属元素,其形成的各种化合物在自然界中广泛存在

(1)Si位于元素周期表第______周期______族;基态硼原子的电子排布式为______;C、N、Si元素原子的第一电离能由大到小的顺序为______。
(2)BF3与一定量的水可形成如图1晶体R,晶体R中各种微粒间的作用力包含______(填字母)。
a.离子键 b.共价键 c.范德华力 d.金属键
(3)乙二胺(H2N﹣CH2﹣CH2﹣NH2)与CuCl2溶液可形成配离子(结构如图2)。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是______。
(4)在25℃、101kpa,NO2(g)与SO2(g)反应生成 SO3(g)和 NO(g),已知每生成1gSO3(g)放出热量 0.52kJ,该反应的热化学方程式是______。
(5)硼砂(Na2B4O710H2O)可用作清洁剂或杀虫剂,易溶于水.在酸性溶液中会生成H3BO3,该反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是
A. 油脂水解的产物中一定含甘油
B. 氨基酸既能与盐酸反应,也能与NaOH反应
C. 糖类、油脂和蛋白质都属于高分子化合物
D. 医疗上用75%的酒精消毒是因为其能使蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 电解池将化学能转化为电能
B. 在原电池的负极和电解池的阴极上都是发生失电子的氧化反应
C. 用惰性电极电解饱和NaCl溶液一段时间后,若 通入氯化氢气体,能使电解液恢复到原状态
D. 用惰性电极电解Na2SO4溶液,阴阳两极气体产物的物质的量之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中含Cl﹣浓度最小的是( )
A.100mL0.25mol/L的NaCl溶液B.30mL0.1mol/L的KCl溶液
C.20mL0.1mol/L的CaCl2溶液D.10mL0.1mol/L的AlCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求对下图中两极进行必要的联接并填空:其中a.b为惰性电极
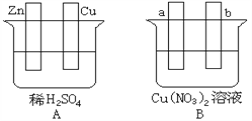
(1)在A图中,使铜片上冒H2气泡,加以必要联接,则联接后的装置叫______。锌片做_____ 极,铜电极上的反应式为_________________;溶液中向锌电极方向移动的离子是___________。
(2)在B图中,使a极析出铜,则b析出O2 ,加以必要的联接后,该装置叫____。装置中发生反应的化学方程式为__________________。经过一段时间后,停止反应并搅均溶液,溶液的酸性会____(增强、减弱、不变),若使溶液恢复至与电解前完全一致,可加入一定量的___________(填序号)。
A. Cu B. CuO C. Cu (OH)2 D. CuCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镓与ⅤA族元素形成的化合物是重要的半导体材料,应用最广泛的是砷化镓(GaAs)。回答下列问题:
(1)基态Ga原子的核外电子排布式为__________,基态As原子核外有__________个未成对电子。
(2)镓失去电子的逐级电离能(单位:kJ·mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为__________和+3。砷的电负性比镓__________(填“大”或“小”)。
(3)比较下列镓的卤化物的熔点和沸点,分析其变化规律及原因:__________________________。
镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
熔点/℃ | 77.75 | 122.3 | 211.5 |
沸点/℃ | 201.2 | 279 | 346 |
GaF3的熔点超过1000℃,可能的原因是_______________________________________。
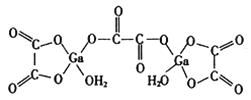
(4)二水合草酸镓的结构如图所示,其中镓原子的配位数为__________,草酸根中碳原子的杂化方式为__________。
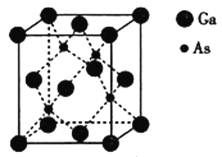
(5)砷化镓熔点为1238℃,立方晶胞结构如图所示,晶胞参数为a=565pm,该晶体的类型为__________,晶体的密度为__________(设NA为阿伏加德罗常数的数值,列出算式即可)g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. Fe2O3溶于氢碘酸:Fe2O3+6H+=2Fe3++3H2O
B. Na2SO3与稀硝酸:SO32-+2H+=SO2↑+H2O
C. AlCl3溶液中加入足量的氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D. Ca(HCO3)2溶液中加入足量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3+CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,同体积的CO和CO2,下列说法不正确的是( )
A.分子数之比等于1:1B.碳原子数之比等于2:3
C.物质的量之比等于1:1D.原子数之比等于2:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com