
下列反应中,调节反应物用量或浓度,或改变反应的温度,不会改变反应产物的是()
①Na与氧气反应②乙醇和浓硫酸共热③二氧化硫通入烧碱溶液 ④硫酸中加入铁粉⑤氨水加入硝酸银溶液 ⑥铁与硝酸溶液 ⑦硫化氢在氧气中燃烧⑧金属钠投入水中.
| A. | ②④⑤ | B. | ①③⑥ | C. | ④⑦ | D. | ⑧ |
| 钠的化学性质;氨的化学性质;硝酸的化学性质;二氧化硫的化学性质;浓硫酸的性质;硫化氢;铁的化学性质;乙醇的化学性质. | |
| 专题: | 元素及其化合物. |
| 分析: | 钠与氧气、乙醇和浓硫酸反应的温度不同,生成物不同; 二氧化硫与氢氧化钠、氨水和硝酸银、硫化氢和氧气反应的量不同,生成物不同; 硫酸与铁、铁与硝酸,硫酸、硝酸的浓度不同,生成物不同; 钠和水反应只生成氢氧化钠和氢气. |
| 解答: | 解:①Na与氧气反应,产温下反应生成氧化钠,加热生成过氧化钠; ②乙醇和浓硫酸共热,140℃生成乙醚,170℃生成乙烯; ③二氧化硫通入烧碱溶液,二氧化硫不足生成亚硫酸钠,二氧化硫过量生成亚硫酸氢钠; ④硫酸中加入铁粉,稀硫酸生成硫酸亚铁和氢气,浓硫酸在加热条件下生成二氧化硫; ⑤氨水加入硝酸银溶液,氨水不足生成氢氧化银,氨水过量生成银氨络离子; ⑥铁与硝酸溶液,稀硝酸生成一氧化氮、浓硝酸生成二氧化氮; ⑦硫化氢在氧气中燃烧,氧气不足生成硫,氧气过量生成二氧化硫; ⑧金属钠投入水中,只生成氢氧化钠和水. 则调节反应物用量或浓度,或改变反应的温度,不会改变反应产物的只有⑧. 故选D. |
| 点评: | 本题综合考查元素化合物知识,为高频考点,题目信息量大,涉及物质种类多,侧重于元素化合物知识的综合理解和运用的考查,难度中等. |


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
下列浓度关系正确的是( )
A.氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)]
B. 氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-)
C.等体积等浓度的氢氧化钠与醋酸混合:c(Na+)=c(CH3COO-)
D.Na2CO3溶液中:c(Na+)>c(CO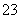 )>c(OH-)>c(HCO
)>c(OH-)>c(HCO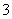 )>c(H+)
)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
10ml浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成的是( )
A.K2SO4 B.CH3COONa C.CuSO4 D.Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.01mol下列物质分别加 入100mL蒸馏水中,恢复至室温,所得溶液中阴离子浓度的大小顺序是(溶液体积变化忽略不计)
入100mL蒸馏水中,恢复至室温,所得溶液中阴离子浓度的大小顺序是(溶液体积变化忽略不计)
①Na2O2②Na2O③Na2CO3④NaCl()
| A. | ①>②>③>④ | B. | ①>②>④>③ | C. | ①=②>③>④ | D. | ①=②>③=④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2CO3固体中可能含有杂质K2CO3、NaHCO3、NaCl中一种或几种,取10.6g样品,加入足量的稀盐酸产生气体4.8g,下列分析正确的是()
| A. | 一定含有NaHCO3 | B. | 一定含有K2CO3 | |
| C. | 一定不含NaCl | D. | 一定含有NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•10H2O),为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验.
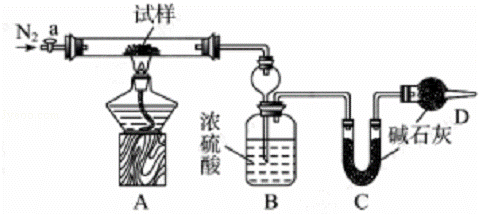
实验过程:
Ⅰ.按图组装仪器,检查装置的气密性;
Ⅱ.将试样m1g放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3g;
Ⅲ.关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
Ⅳ.称得装置B的质量为m4g、装置C的质量为m5g.
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为,.
(2)装置B的作用为.装置C的作用为.
(3)实验过程中通入N2的目的 为.
为.
(4)用下列各项所提供的数据能计算出w(NaHCO3)的是bce(填选项字母)
| 序号 | a | b | c | d | e |
| 数据 | m1,m2,m3 | m2,m3,m4,m5 | m1,m2,m4 | m1,m4,m5 | m1,m3,m5 |
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的w(NaHCO3),若能,则w(NaHCO3)的计算式为:×100%(若不能,此问不作答.)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2(g)+F2(g)===2HF(g) ΔH=-270 kJ·mol-1,下列说法正确的是( )
A.2 L氟化氢气体分解成1 L氢气与1 L氟气吸收270 kJ热量
B.1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ
C.在相同条件下,1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列三个热化学方程式
①H2(g)+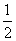 O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
③C(s)+H2O(g)===CO(g)+H2(g)
ΔH=+131 kJ·mol-1
写出碳燃烧生成CO和CO燃烧的热化学方程式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com