
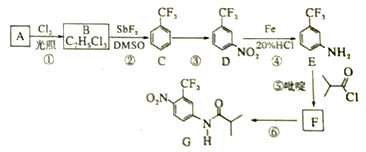
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:
回答下列问题:
(1)A的结构简式为_______________。C的化学名称是________________________。
(2)③的反应试剂和反应条件分别是______________________,该反应的类型是___________。
(3)⑤的反应方程式为_____________________________________________。
吡啶是一种有机碱,其作用是______________________________。
(4)G的分子式为______________________________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则Ⅱ可能的结构有_________种。
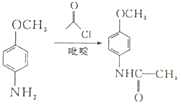
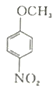
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备小甲氧基乙酸苯胺的合成路线(其他试剂任选)_______________。
)制备小甲氧基乙酸苯胺的合成路线(其他试剂任选)_______________。
【答案】![]() 三氟甲苯 浓
三氟甲苯 浓![]() /浓
/浓![]() ,加热 取代反应 见解析 吸收反应产生的HCl,提高反应转化率
,加热 取代反应 见解析 吸收反应产生的HCl,提高反应转化率 ![]() 9
9 
![]()
![]()
【解析】
根据官能团的结构和性质分析解答;根据题目信息流程正向、逆向进行分析解答。
由C 三氟甲苯结构简式逆向推理可知B为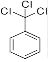 ,即A为
,即A为![]() ,C发生硝化反应生成D,D中硝基被还原成氨基,生成E,E发生消去反应得到F:
,C发生硝化反应生成D,D中硝基被还原成氨基,生成E,E发生消去反应得到F: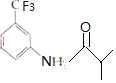 ,进而F发生硝化反应生成G;
,进而F发生硝化反应生成G;
(1)由C:三氟甲苯结构简式逆向推理可知B为 ,即A为
,即A为![]() ,故答案为:
,故答案为:![]() ;三氟甲苯;
;三氟甲苯;
(2)反应③是E发生在浓硫酸做催化剂的加热的条件下与硝酸发生硝化反应,故答案为:浓![]() /浓
/浓![]() ,加热;
,加热;
(3)反应⑤中吡啶的作用是吸收反应产生的氯化氢,提高反应转化率,反应方程式为 ,故答案为:吸收反应产生的氯化氢,提高反应转化率;
,故答案为:吸收反应产生的氯化氢,提高反应转化率;
(4)由G结构简式可知,G的分子式为C11H11F3N2O3,故答案为:C11H11F3N2O3;
(5)H是G的同分异构体,其取代基相同但位置不同,故H中三氟甲基和硝基有邻间对3种位置关系,邻位时,另一基团有4种位置;间位时,另一基团有4种位置,对位时,另一基团有2种位置;除去G,则H有9种可能;故答案为:9;
(6)根据题给流程图分析,苯甲醚首先在对位加硝基,然后硝基氢化,氢化后再在吡啶存在的条件下和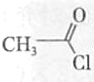 反应得到目标产物,流程为:
反应得到目标产物,流程为: 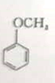
![]()
![]()
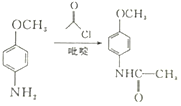 。
。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 0.1mol氯气通入水中,转移电子的数目为0.1NA
B. 常温常压下,7.8g过氧化钠含有阴离子的数目为0.2NA
C. 标准状况下,22.4LCl2与足量的铁充分反应,转移电子数为3NA
D. 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 按系统命名法,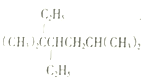 的名称为3,3,6一三甲基-4-乙基庚烷
的名称为3,3,6一三甲基-4-乙基庚烷
B. 已知C-C键可以绕键轴自由旋转,结构简式为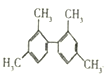 的分子中至少有11个碳原子处于同一平面上
的分子中至少有11个碳原子处于同一平面上
C. 苯中含有杂质苯酚,可用浓溴水来除杂
D. 1mol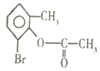 ,在一定条件下与足量NaOH溶液反应,最多消耗3molNaOH
,在一定条件下与足量NaOH溶液反应,最多消耗3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,已知醋酸的电离常数为1.75×10-5,向20mL0.01mol·L-1CH3COOH溶液中逐滴加入0.01mol·L-1的NaOH溶液,溶液中水电离的c(H+)随加入NaOH溶液的体积变化如图所示,下列说法正确的是(已知![]() =4.2)
=4.2)
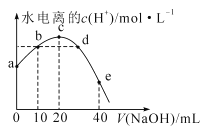
A.b、d两点溶液的pH相同
B.b点溶液中离子浓度大小顺序是:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.e点所示溶液中,c(Na+)=2[c(CH3COO-)+c(CH3COOH)]=0.005mol/L
D.a点坐标为(0,2.4×10-11)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PBS是一种可降解的聚酯类高分子材料,可由马来酸酐等原料经下列路线合成:

(已知:![]() +
+
![]()
 )
)
(1)A→B的反应类型是____________;B的结构简式是______________________。
(2)C中含有的官能团名称是________;D的名称(系统命名)是____________。
(3)半方酸是马来酸酐的同分异构体,分子中含1个环(四元碳环)和1个羟基,但不含—O—O—键。半方酸的结构简式是___________________。
(4)由D和B合成PBS的化学方程式是______________________________________。
(5)下列关于A的说法正确的是__________。
a.能使酸性KMnO4溶液或溴的CCl4溶液褪色
b.能与Na2CO3反应,但不与HBr反应
c.能与新制Cu(OH)2反应
d.1molA完全燃烧消耗5molO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃,101kPa下,lg C8H18(辛烷)(相对分子质量:114)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是( )
A. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(g);△H=-48.40kJ·mol-1
B. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1);△H=-5518kJ·mol-1
C. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1);△H=+5518kJ·mol-1
D. C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1);△H=-48.40kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.22.4L氢气中含有的氢分子数目为NA
B.标准状况下,4.48L水中含有的水分子数目为0.2NA
C.常温常压下,14g氮气含有的氮原子数目为NA
D.0.2mol·L-1CaCl2溶液中含有的氯离子数目为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中充入NO2,发生反应2NO2(g)![]() N2O4(g)。其它条件相同时,不同温度下平衡体系中各物质的物质的量分数如下表:(已知:N2O4为无色气体)
N2O4(g)。其它条件相同时,不同温度下平衡体系中各物质的物质的量分数如下表:(已知:N2O4为无色气体)
t/℃ | 27 | 35 | 49 | 70 |
NO2% | 20 | 25 | 40 | 66 |
N2O4% | 80 | 75 | 60 | 34 |
下列说法不正确的是( )
A.27℃,该平衡体系中的NO2转化率为![]()
B.平衡时,NO2的消耗速率为N2O4消耗速率的2 倍
C.室温时,将盛有NO2的密闭玻璃球放入冰水中其颜色会变浅
D.其他条件不变,增大NO2起始量,平衡正移,该反应的化学平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容容器中,当下列物理量不再发生变化时:①混合气体的压强;②混合气体的密度;③混合气体的总物质的量;④混合气体的平均相对分子质量;⑤混合气体的颜色;⑥各反应物或生成物的浓度之比等于化学计量数之比;⑦某种气体的百分含量。能说明A(s)![]() 3B(g)+C(g)达到平衡状态的是( )
3B(g)+C(g)达到平衡状态的是( )
A. ①②③④
B. ①②③④⑦
C. ①③④⑦
D. ①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com