
用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量相应的溶质能使溶液恢复到电解前浓度的是( )
A.AgNO3 B.Na2SO4 C.CuCl2 D.KCl
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A. 浓硝酸和浓硫酸露置于空气中,容器内酸液的浓度都降低
B. 可用铁制容器储存稀硝酸
C. SO2溶于水生成H2SO4
D. SO2通入BaCl2溶液中能产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
对于合成氨的反应,使用催化剂和施加高压,下列叙述中,正确的是( )
A.都能提高反应速率,都对化学平衡状态无影响
B.都对化学平衡状态有影响,都不影响达到平衡状态所用的时间
C.都能缩短达到平衡状态所用的时间,只有压强对化学平衡状态有影响
D.催化剂能缩短反应达到平衡状态所用的时间,而压强无此作用
查看答案和解析>>
科目:高中化学 来源: 题型:
AgCl和Ag2CrO4的溶度积分别为1.8×10-10 mol2·L-2和2.0×10-12 mol3·L-3,若用难溶盐在溶液中的浓度来表示其溶解度,则下面的叙述中正确的是( )
A.AgCl和Ag2CrO4的溶解度相等
B.AgCl的溶解度大于Ag2CrO4的溶解度
C.两者类型不同,不能由Ksp的大小直接判断溶解能力的大小
D.都是难溶盐,溶解度无意义
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解下列溶液一段时间后再加入一定量的某种纯净物(方括号内的物质),能使溶液恢复到原来的成分和浓度的是( )
A.AgNO3[AgNO3] B.NaOH[H2O] C.KCl[KCl] D.CuSO4[Cu(OH)2]
查看答案和解析>>
科目:高中化学 来源: 题型:
下图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336 mL (标准状况)气体。回答:
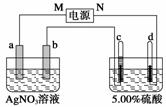
(1)直流电源中,M为__________极。
(2)Pt电极上生成的物质是________,其质量为__________________________g。
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为2∶______∶______∶________。
(4)AgNO3溶液的浓度________(填“增大”、“减小”或“不变”,下同),AgNO3溶液的pH______,硫酸的浓度__________________________,硫酸的pH________。
(5)若硫酸的质量分数由5.00%变为5.02%,则原有5.00%的硫酸________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液。通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是( )
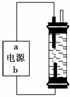
A.a为正极,b为负极;NaClO和NaCl
B.a为负极,b为正极;NaClO和NaCl
C.a为阳极,b为阴极;HClO和NaCl
D.a为阴极,b为阳极;HClO和NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
在25℃时,将pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合后,下列关系式中正确的是( )
A.[Na+]=[CH3COO-]+[CH3COOH]
B.[H+]=c(CH3COO-)+[OH-]
C.[Na+]>[CH3COO-]>[OH-]>[H+]
D.[CH3COO-]>[Na+]>[H+]>[OH-]
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A(g)+B(g)C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K=________,ΔH________0(填“<”、“>”或“=”);
(2)830℃时,向一个5 L的密闭容器中充入0.20 mol的A和0.80 mol的B,如反应初始6 s内A的平均反应速率v(A)=0.003 mol·L-1·s-1,则6 s时c(A)=________ mol·L-1,C的物质的量为________mol;反应经一段时间,达到平衡时A的转化率为________,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为________;
(3)判断该反应是否达到平衡的依据为________(填正确选项前的字母);
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
(4)1 200℃时反应C(g)+D(g)A(g)+B(g)的平衡常数的值为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com