
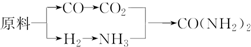
分析 (1)温度影响化学反应速率及化学平衡;工业生产中,以氨气为原料合成硝酸,是先将氨催化氧化生成一氧化氮,一氧化氮与氧气反应生成二氧化氮,二氧化氮与水反应生成硝酸,据此写化学方程式;
(2)用原料所制得的H2和CO2的物质的量之比若最接近合成尿素的原料气NH3(换算成H2的物质的量)和CO2的物质的量之比,原料的利用率最高,根据原料气产生的H2和CO2的物质的量之比判断;
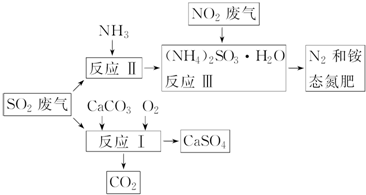
(3)①根据反应物和生成物,写出反应Ⅰ的化学方程式;
②加入强还原性的对苯二酚等物质,目的是防止亚硫酸铵(NH4)2SO3被氧化;
③检验SO42-所用试剂是盐酸和氯化钡;
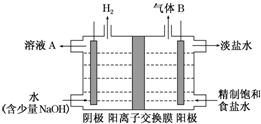
(4)①二氧化硫和氢氧化钠反应生成NaHSO3;
②阳极区产生的气体氯气的溶液与二氧化硫发生氧化还原反应.
解答 解:(1)合成氨反应的化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ/mol,在400~500℃的高温时,催化剂的催化活性最强,同时升高温度虽然不利于平衡向正反应方向移动,但能增大反应速率,缩短达到平衡的时间;工业生产中,以氨气为原料合成硝酸,是先将氨催化氧化生成一氧化氮,一氧化氮与氧气反应生成二氧化氮,二氧化氮与水反应生成硝酸,所以工业生产硝酸的最后一步的化学方程式为3NO2+H2O=2HNO3+NO,
故答案为:催化活性最强,增加反应速率,缩短达到平衡的时间; 3NO2+H2O=2HNO3+NO;
(2)NH3(换算成H2的物质的量)和CO2的物质的量之比为2:1合成尿素,即H2和CO2的物质的量之比为$\frac{2×3}{2}$:1=3:1.
甲厂以焦炭和水为原料,C+2H2O$\frac{\underline{\;高温\;}}{\;}$CO2+2H2,生成的H2和CO2的物质的量之比为2:1.
乙厂以天然气和水为原料,CH4+2H2O$\frac{\underline{\;高温\;}}{\;}$CO2+4H2,生成的H2和CO2的物质的量之比为4:1.
丙厂以石脑油和水为原料,C5H12+10H2O$\frac{\underline{\;高温\;}}{\;}$5CO2+16H2,生成的H2和CO2的物质的量之比为16:5,丙最接近3:1,
故答案为:丙;
(3)①根据反应物和生成物,写出反应Ⅰ的化学方程式为:2CaCO3+O2+2SO2=2CaSO4+2CO2,
故答案为;2CaCO3+O2+2SO2=2CaSO4+2CO2;
②亚硫酸根离子易被氧化,向反应Ⅱ的溶液中加入强还原性的对苯二酚等物质,目的是防止亚硫酸铵(NH4)2SO3被氧化,
故答案为:防止亚硫酸铵(NH4)2SO3被氧化;
③检验SO42-所用试剂是盐酸和氯化钡(HCl 和 BaCl2),
故答案为:盐酸和氯化钡(HCl 和 BaCl2);
(4)①二氧化硫和氢氧化钠反应生成NaHSO3,SO2+OH-=HSO3-(或SO2+2OH-=SO32-+H2O),
故答案为:SO2+OH-=HSO3-(或SO2+2OH-=SO32-+H2O);
②阳极区产生的气体氯气的溶液与二氧化硫发生氧化还原反应,SO2+Cl2+H2O=4H++SO42-+2Cl-,
故答案为:SO2+Cl2+H2O=4H++SO42-+2Cl-.
点评 本题考查了影响化学反应速率的因素,化学方程式的计算,离子反应等,考查的知识点较多,结合性强,题目难度中等,试题能够提高学生的分析、理解能力及计算能力.


 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:解答题
 ;反应类型:加聚反应.
;反应类型:加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素位于元素周期表的第三周期ⅦA族 | |
| B. | 生成的盐含有的化学键既有离子键又有共价键 | |
| C. | 该元素的常见化合价有:-1、0、+1、+3、+5、+7等 | |
| D. | 该元素的氢化物的稳定性比PH3、H2S弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28 g C2H4所含共用电子对数目为4NA | |
| B. | 1 L 0.1 mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 1 mol甲烷分子所含质子数为10NA | |
| D. | 标准状况下,22.4 L乙醇的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
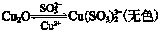
| 操作 | 现象 |
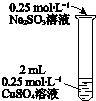 | i 有黄色沉淀出现,随着 Na2SO3溶液的滴入,沉淀增加,当加到5mL时,溶液的蓝色消失. ii 将试管加热,黄色沉淀变为砖红色,有刺激性气味气体产生. iii在加热条件下,继续滴入Na2SO3溶液,砖红色沉淀减少,当1加到10mL时,沉淀完全溶解,得无色溶液. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制取乙炔时,用饱和食盐水代替蒸馏水,以得到平稳的气流 | |
| B. | 除去苯中的少量苯酚:加入适量NaOH溶液,振荡、静置、分液 | |
| C. | 液态溴乙烷中加入稀NaOH溶液共煮几分钟,然后加入足量稀硝酸,再加入AgNO3溶液检验溴乙烷中是否含有溴元素 | |
| D. | 检验甲酸中是否混有乙醛,可向样品中加入足量NaOH溶液以中和甲酸,再做银镜反应或与新制Cu(OH)2共热的实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
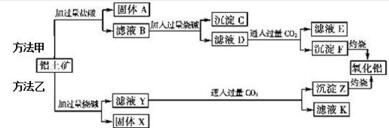
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com