
【题目】现代传感信息技术在化学实验中有广泛的应用。某小组用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理(如图1 所示),并测定电离平衡常数Kb。

(1)实验室制取氨气的化学方程式为_____________;
图1 中用浓氨水和X 固体快速制取NH3,X固体不可以是________(填序号)
A.生石灰 B.无水氯化钙 C.烧碱 D.碱石灰
(2)关闭a,将带有装满水的胶头滴管的橡皮塞塞紧c 口,_______(填操作)可引发喷泉实验,电脑绘制三颈瓶内气压变化曲线如图2 所示。图2中________点时喷泉喷的最剧烈。
(3)喷泉实验结束后,发现水未充满三颈烧瓶(大约占体积的90 % ) ,如装置的气密性良好,烧瓶未充满水的原因是________________,所得氨水的物质的量浓度为________。
(4)从三颈瓶中用__________(填仪器名称)量取25. 00 mL氨水至锥形瓶中,用0.0500mol/LHCl 滴定测定氨水的浓度。用pH 计采集数据、电脑绘制滴定曲线如图3 所示。

当pH=11.0时,NH3·H2O电离平衡常数Kb的近似值,Kb≈_________。
(5)关于该滴定实验的说法中,正确的是_______(填序号)
A. 锥形瓶中有少量蒸馏水不影响测定结果
B.选择酚酞作为指示剂,测定结果偏高
C.酸式滴定管未用盐酸润洗会导致测定结果偏低
D.滴定终点时俯视读数会导致测定结果偏高
【答案】(15分)(1)2NH4Cl+Ca(OH)2![]() CaCl2+2H2O+2NH3↑;(2分)B(1分);
CaCl2+2H2O+2NH3↑;(2分)B(1分);
(2)打开b,挤压胶头滴管使水进入烧瓶;(2分)C(1分);
(3)氨气中混有空气(2分);0.045mol/L(1分);
(4)碱式滴定管(或20mL移液管)(2分);2.2×10-5(2分);
(5)A(2分);
【解析】
试题分析:(1)利用消石灰与NH4Cl固体混合加热制氨气,发生反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2H2O+2NH3↑;浓氨水易挥发,生石灰、烧碱和碱石灰溶于,水与水反应放出大量的热,能够促进氨气的逸出,而无水氯化钙能够与氨气反应,所以不能用来制氨气;
CaCl2+2H2O+2NH3↑;浓氨水易挥发,生石灰、烧碱和碱石灰溶于,水与水反应放出大量的热,能够促进氨气的逸出,而无水氯化钙能够与氨气反应,所以不能用来制氨气;
故答案为B;
(2)要形成喷泉实验,应使瓶内外形成负压差,而氨气极易溶于水,所以打开b,挤压胶头滴管使水进入烧瓶,氨气溶于水,使瓶内压强降低,形成喷泉;三颈瓶内气体与外界大气压压强之差越大,其反应速率越快,C点压强最小、大气压不变,所以大气压和C点压强差最大,则喷泉越剧烈;
(3)装置的气密性良好,烧瓶未充满水说明氨气中混有空气,假设氨气的体积为VL,则氨水的体积也为VL,氨气的物质的量为VL÷22.4L/mol=V/22.4mol,所得氨水的物质的量浓度为V/22.4mol÷VL=0.045mol/L;
(4)氨水显碱性,量取碱性溶液,应选择碱式滴定管;氨水的物质的量浓度为0.045mol/L,pH=11的氨水中c(OH-)=0.001mol/L,c(OH-)≈c(NH4+)=0.001mol/L,c(NH3H2O)≈0.0450mol/L,根据Kb=![]() ==2.2×10-5;
==2.2×10-5;
(5)A.锥形瓶中有少量蒸馏水不影响氨水的物质的量,所以不影响测定结果,故A正确;B.酚酞为碱性指示剂,滴定终点时消耗盐酸的体积偏低,测定浓度偏低,故B错误;C.酸式滴定管未用盐酸润洗会导致盐酸浓度偏低,则使用盐酸的体积偏大,所以导致测定结果偏高,故C错误;D.滴定终点时俯视读数会导致盐酸体积偏小,则盐酸物质的量偏小,测定结果偏低,故D错误;故选A。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】工业上回收利用某合金废料(主要含Fe、Al、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:
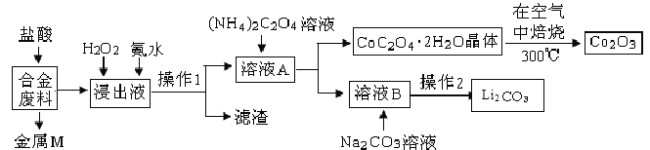
(1) 金属M为 ,操作1所用的玻璃仪器除烧杯外还有 。
(2) 加入H2O2的作用是 (用离子方程式表示),加入氨水的作用是 。
(3) 在空气中焙烧的化学方程式为 。
(4) 已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表。操作2中,蒸发浓缩后必须趁热过滤,其原因是 。
温度/℃ | 10 | 30 | 60 | 90 |
浓度/mol·L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
(5) 用惰性电极电解熔融Li2CO3制取锂,阳极生成两种气体,则阳极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】垃圾无害化处理首先要求将垃圾分类收集。某居民小区垃圾收集点有三个垃圾桶,分别标明“厨余垃圾”、“电池”、“可回收物”。下列物质中不应投入“可回收物”桶内的是
A. 玻璃碎片 B. 破塑料盒 C. 纸制包装盒 D. 瓜皮果壳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列烷烃的沸点是
物质 | 甲烷 | 乙烷 | 丁烷 | 戊烷 |
沸点 | —162℃ | —89℃ | —1℃ | +36 ℃ |
根据以上数据推断丙烷的沸点可能是
A.约—40℃ B.低于—162 ℃
C.低于—89℃ D.高于+36℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体A 在一定温度下分解生成气体B、C、D:2A=B+2C+3D,若测得生成气体的质量是相同体积H2的15倍,则固体A的摩尔质量是
A.30g · mol-1 B.60g · mol-1 C.90g · mol-1 D.120g · mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,横轴为溶液的pH,纵轴为Zn2+或ZnO22-物质的量浓度的对数。回答下列问题:
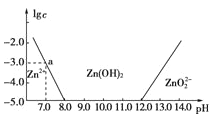
(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为__________。
(2)从图中数据计算可得Zn(OH)2的溶度积Ksp=________________。
(3)某废液中含Zn2+,为提取Zn2+可以控制溶液pH的范围是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应或对事实解释的离子方程式不正确的是
A.盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-=SiO32-+H2O
B.双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O
C.用铜作电极电解CuSO4溶液:2Cu2++2H2O![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D.消毒液与洁厕灵(主要成分是HCl)混用,产生有毒Cl2:2H++Cl-+ClO-=Cl2+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班化学兴趣小组做如下实验,请你回答相关问题:
Ⅰ、甲组同学想用金属钠和空气制备纯度较高的Na2O2(不考虑空气中N2),可利用的装置如下。回答下列问题:
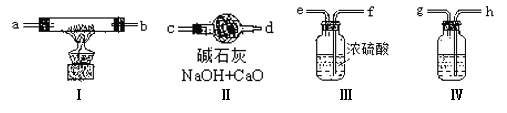
(1)装置Ⅳ中盛放的药品是 ,若没有该装置可能导致生成的Na2O2中含有 ,其反应方程式为 。
(2)若规定气体的气流方向从左到右,各仪器接口的标号字母(a、b……)顺序是:
空气进入 , 接 , 接 , 接 。
(3)装置的Ⅱ作用是 。
Ⅱ、乙组利用下图所示实验装置进行某些气体的制备、性质等试验(图中夹持装置有省略)。
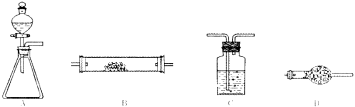
(4)为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A-C-B-D连接成实验装置体系。A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是 ;A中发生的化学方程式是 ,C中试剂是 ,D的作用是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com