
【题目】常温下,将1.0 mol/L 盐酸滴入20 mL 1.0 mol/L氨水中,溶液pH随加入盐酸体积变化的曲线如图所示。下列有关说法正确的是( )
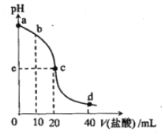
A.a点,c(NH4+)=c(OH-)
B.b点,c(NH4+)>c(Cl-)>c(NH3·H2O)
C.c点,pH=7
D.d点,c(NH4+)+c(NH3·H2O)=c(Cl-)
【答案】B
【解析】
A.a点为氨水溶液,溶液中存在电荷守恒,c(NH4+)+c(H+)=c(OH-),则c(NH4+)<c(OH-),A错误;
B.b点,2n(HCl)=n(氨水),二者反应后溶液中溶质为等物质的量浓度的NH4Cl、NH3H2O,溶液呈碱性,说明NH3H2O的电离程度大于NH4Cl的水解程度,但其水解程度和电离程度都较小,所以溶液中存在c(NH4+)>c(Cl-)>c(NH3·H2O),B正确;
C.c点二者恰好完全反应生成NH4Cl,NH4Cl是强酸弱碱盐,其水溶液呈酸性,则pH<7,C错误;
D.d点,n(HCl)=2n(氨水),二者反应后溶液中溶质为等物质的量浓度的HCl、NH4Cl,溶液中存在物料守恒,根据物料守恒得2c(NH4+)+2c(NH3·H2O)=c(Cl-),D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
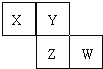
A.原子半径:W > Z > Y > X
B.最高价氧化物对应水化物的酸性:Z > W
C.4种元素的单质中Z单质的熔、沸点最低
D.W单质能与水反应生成一种具有漂白性的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,按下列物质的量关系进行反应,其对应的离子方程式或化学方程式书写正确的是
A.n(Cl2)∶n(Fe)=5∶4;5Cl2+4Fe![]() 2FeCl2+2FeCl3
2FeCl2+2FeCl3
B.n(Cl2)∶n(FeBr2)=1∶1;Fe2++2Br+Cl2=Fe3++Br2+2Cl
C.n(MnO4-)∶n(H2O2)=2∶3;2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
D.n(Fe) ∶n[HNO3(稀)]=1∶3;4Fe+12H++3NO3-=3Fe2++Fe3++3NO↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学利用如图所示实验装置进行实验(图中a、b、c)表示止水夹。
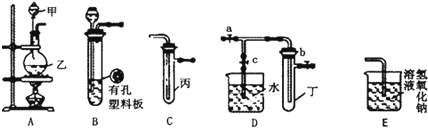
请按要求填空:(可供选择的试剂有:Cu片,MnO2粉末,浓硝酸,稀硝酸,浓硫酸,浓盐酸,氢氧化钠溶液,酚酞)
(1)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。若在丙中加入适量水,即可制得氯水。将所得氯水加入到滴有酚酞的NaOH溶液中,观察到溶液褪色,甲同学给出的结论是氯水溶于水生成了酸,将NaOH中和后溶液褪色。
a.写出制取氯气的化学方程式:___。
b.乙同学认为甲同学的结论不正确,他认为褪色的原因可能是___。
c.如何验证甲、乙两同学的结论(写出所加试剂,现象,结论):___。
(2)B、D、E装置相连后,可制得NO2并进行有关实验。
①B中发生反应的化学方程式为___。
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹___,再打开止水夹___,使烧杯中的水进入试管丁的操作是___。
③试管丁中的NO2与水充分反应,若向试管内缓缓通入一定量的O2,直到试管全部充满水,则所得溶液中的溶质的物质的量浓度是___(气体按标准状况计算,结果保留二位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是在实验室进行氨气快速制备与性质实验的组合装置,部分固定装置未画出。
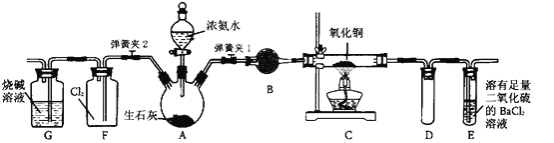
(1)在组装好装置后,若要检验A~E装置的气密性,其操作是首先____,然后微热A,观察到E中有气泡冒出,移开酒精灯或松开双手,E中导管有水柱形成,说明装置气密性良好。
(2)装置B中盛放的试剂是________。
(3)点燃C处酒精灯,关闭弹簧夹2,打开弹簧夹l,从分液漏斗放出浓氨水至浸没烧瓶中固体后关闭分液漏斗,稍候片刻,装置C中黑色固体逐渐变红,装置E中溶液里出现大量气泡,同时还可能产生的现象是________;从E中逸出液面的气体可以直接排入空气,请写出在C中发生反应的化学方程式:________。
(4)当C中固体全部变红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量,若反应前固体质量为16 g,反应后称重固体质量减少2.4 g,通过计算确定该固体产物的成分是________(用化学式表示)。
(5)在关闭弹簧夹1后,打开弹簧夹2,残余气体进入F中,很快发现装置F中产生白烟,同时发现G中溶液迅速倒吸流入F中。请写出产生白烟的化学方程式:________,迅速产生倒吸的原因是________。
(6)为了汪明一水合氨是弱碱,甲、乙两同学分别设计以下实验进行探究。
①甲同学用pH试纸测得室温下0.l mol/L氨水pH为10,则认定一水合氨是弱电解质,理由是________。
②乙同学取出10 mL 0.1 mol/L氨水,滴入2滴酚酞试液,显粉红色,再加入NH4Cl晶体少量,观察到的现象是________,则证明一水台氨是弱电解质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将淀粉水解并用新制Cu(OH)2悬浊液检验水解产物的实验中,要进行的主要操作有:①加热;②滴入稀硫酸;③加入新制的Cu(OH)2悬浊液;④加入NaOH溶液中和。以上各步操作的先后顺序排列正确的是________。
A.②③④① B.②④③① C.②①④③ D.④③②①
(2)若某学生称取9g淀粉溶于水,按以下步骤做淀粉水解实验,回答下列问题。

①写出淀粉水解的化学方程式:________________。
②沉淀的单质是________________(写化学式)。
③填写所加试剂名称及其作用:
A________,作用________________________________;
B________,作用________________________________。
④当析出3.24g单质沉淀时,淀粉的水解率为________(已知1mol醛基发生银镜反应时生成2molAg)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下图装置制备家用消毒液,并探究其性质。
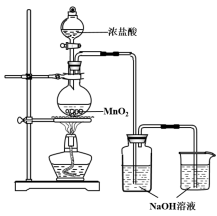
反应停止后,取洗气瓶中无色溶液5mL分别进行了如下实验:
操作 | 现象 |
a. 测溶液pH, 并向其中滴加2滴酚酞 | pH = 13, 溶液变红,5min后褪色 |
b. 向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
(1)写出利用上述装置制备消毒液涉及反应的化学方程式 、 。
(2)查阅资料:酚酞的变色范围为8.2~10,且酚酞在强碱性溶液中红色会褪去
为探究操作a中溶液褪色的原因,又补充了如下实验:
操作 | 现象 |
取 NaOH溶液,向其中滴加2滴酚酞 | 溶液变红,30min后褪色 |
获得结论:此实验小组制备的消毒液具有 性。
(3) 该小组由操作b获得结论:随着溶液酸性的增强,此消毒液的稳定性下降。
① 操作b中溶液变成黄绿色的原因: (用离子方程式表示)。
② 有同学认为由操作b获得上述结论并不严谨,需要进一步确认此结论的实验方案是 。
(4) 有效氯的含量是检测含氯消毒剂消毒效果的重要指标。具体用“单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量”进行表征,一般家用消毒液有效氯含量在5%以上。小组同学进行如下实验测定有效氯:取此消毒液5 g,加入20 mL 0.5 mol·L-1 KI溶液,10 mL 2 mol·L-1的硫酸溶液;加几滴淀粉溶液后,用0.1 mol·L-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3 20 mL。(已知:2S2O32- + I2 === S4O62- + 2I-) 。注:相对原子质量Cl35.5,Na23,S32,O 16 ,I 127, K39
①达到滴定终点时的实验现象是 。
②此消毒液有效氯含量为 %(保留一位有效数字)。获得结论:此实验制得的消毒液 (填“符合”或“不符合”)家用要求。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg5Al3(OH)19(H2O)4![]() 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据____________。
(2)用离子方程式表示除去固体产物中Al2O3 的原理________。
Ⅱ.磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
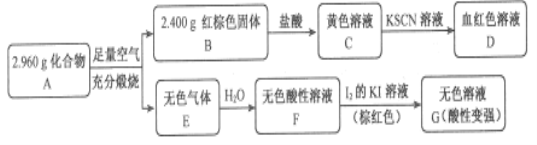
请回答:
(1)A的组成元素为_________(用元素符号表示),化学式为______。
(2)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L-1),写出该反应的离子方程式_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,不能达到相应实验目的的是
实验方案 |
|
|
|
|
实验目的 | A.制备乙酸乙酯 | B.制取新制的 Cu(OH)2溶液 | C.除去溴苯中的苯 | D.除去乙烯中的二氧化硫 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com