
【题目】短周期金属元素甲~戊在周期表中的相对位置如右表所示,下面判断不正确的是( )
甲 | 乙 | |
丙 | 丁 | 戊 |
A. 原子半径: 丙>丁>戊 B. 金属性:甲<丙
C. 最外层电子数:甲>乙 D. 氢氧化物碱性:丙>丁>戊
科目:高中化学 来源: 题型:
【题目】在有机物分子中,若某个碳原子连接4个不同的原子或原子团,则这种碳原子称为“手性碳原子”,凡有一个手性碳原子的物质一定具有光学活性。已知某有机物结构如下:具有光学活性,当它发生下列反应后生成的有机物仍然具光学活性的是
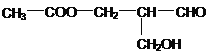
A. 与NaOH溶液共热 B. 与甲酸发生酯化反应
C. 与氧气发生催化氧化 D. 在催化剂存在下与H2作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. SO2和SO3都是酸性氧化物,二者的水溶液都是强酸
B. 将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化
C. 硫粉在适量的纯氧中燃烧可以生成大量的SO3
D. 富含硫磺的矿物在工业上可用于制造硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应均为放热反应,其中反应热最小的是
A.2A(l) + B(l) = 2C (g) △H1
B.2A(g) + B(g) = 2C(g) △H2
C.2A (g) + B ( g ) = 2C(l) △H3
D.2A (l) + B(l)= 2C(l) △H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有的离子可能是K+、Ba2+、Al3+、Mg2+、AlO![]() 、CO
、CO![]() 、SiO
、SiO![]() 、Cl-中的几种,现进行如下实验:
、Cl-中的几种,现进行如下实验:
①取少量溶液加氢氧化钠溶液过程中无沉淀生成
②另取少量原溶液,逐滴加入5 mL 0.2 mol·L-1盐酸,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失。
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到白色沉淀。
下列说法中正确的是( )
A. 该溶液中一定不含Ba2+、Mg2+、Al3+、SiO![]() 、Cl-
、Cl-
B. 该溶液中一定含有K+、AlO![]() 、CO
、CO![]() 、Cl-
、Cl-
C. 该溶液是否有K+需做焰色反应(透过蓝色钴玻璃片)
D. 可能含有Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两种有机物Q(![]() )与P(
)与P(![]() ),下列有关它们的说法中正确的是( )
),下列有关它们的说法中正确的是( )
A. 二者的核磁共振氢谱中均只出现两种峰且峰面积之比为3∶2
B. 二者在NaOH醇溶液中均可发生消去反应
C. 一定条件下,二者在NaOH溶液中均可发生取代反应
D. Q的一氯代物只有1种、P的一溴代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mlbmol·L-1的CH3COOH溶液中滴加等体积的0.01mol·L-1的NaOH溶液,充分反应后溶液中c(CH3COO-)=c(Na+),下列说法不正确的是
A. b>0.01
B. 混合后溶液呈中性
C. CH3COOH的电离常数Ka=![]()
D. 向CH3COOH溶液中滴加NaOH溶液的过程中,水的电离程度逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I实验室用NaOH固体配制1.0mol/L的NaOH溶液450mL,回答下列问题:
(1)实验步骤:
①计算所需称量的NaOH的质量为________g。
②用托盘天平称量NaOH固体。称量时应该将NaOH放于_____中且放置在天平左盘称量。
③将称得的固体放于烧杯中,并加水溶解。
④检查容量瓶是否漏水,用玻璃棒引流将溶解液立即转移进_______mL容量瓶中。
⑤用少量水洗涤______________2-3次;并将洗涤液转移进容量瓶。
⑥定容操作为_________________。
⑦翻转摇匀后转入试剂瓶中储存。
II若配制1mol/L的稀硫酸溶液500 mL则需要质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为_______mL(计算结果保留一位小数)。如果实验室有10mL、25mL、50mL量筒,就选用______mL规格的量筒最好。
(2)下面操作造成所配稀硫酸浓度偏高的是______(填序号)
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com