
����Ŀ����ʽ̼��ͭ[xCuCO3��yCu(OH)2]���ʿ�ȸ����ɫ.�ֳ�Ϊ��ȸʯ����һ������Ŀ��ﱦʯ������ͭ������е�������������̼��ˮ���������ʷ�Ӧ���������ʡ�CuSO4��Һ��Na2CO3��Һ��Ӧ���Եõ���ʽ̼��ͭ�����ǽ�������ɽ������̽����
[�����Ʊ�]��ȡ12. 5 g����(CuSO4 5H2O)����87. 5mL����ˮ�У��μ�����ϡ����(������Ժ��Բ���)����ֽ����õ�CuSO4��Һ�������м���Na2CO3��Һ������������ɫ����Һ���ˣ���������ˮϴ�ӣ�������ˮ�Ҵ�ϴ�ӣ������º�ɱ��á�
[ʵ��̽��]�������������װ�ã����Ƶõ�����ɫ�������ʵ�顣

��������ʵ��ش���������
��1����������ͭ��Һ�Ĺ����еμ�ϡ�����������_______________________________��
��������ͭ��Һ��������������Ϊ_____________________��
��2��ʵ����ͨ��ʹ�ü����������ƺ��Ȼ�炙����Һ�ķ�����ȡN2���÷�Ӧ�Ļ�ѧ����Ϊ��__________________________________________________��
��3��Dװ�ü���ǰ����Ҫ���ȴ���K��ͨ������N2��Ȼ��ر�K���ٵ�ȼD���ƾ��ơ�
C��ʢװ���Լ�Ӧ��___________������D��۲쵽��������_______________________��
��4������������֪��Ksp[CaCO3]=2.8��10-9��Ksp[BaCO3]=5.1��10-9����������Ϊ��Ҫ��Ba(OH)2��Һ�������ʯ��ˮ�������ⶨ����ɫ����Ļ�ѧʽ����ԭ������____��
a.Ba(OH)2�ļ��Ա�Ca(OH)2ǿ
b.Ba(OH)2�ܽ�ȴ���Ca(OH)2���ܳ������CO2
c.��ͬ�����£�CaCO3���ܽ�����Դ���BaCO3
d.���յ���CO2���ɵ�BaCO3����������CaCO3���������С
��5����D�з�Ӧ��ȫ����K���ٴεμ�NaNO2��Һ����N2����Ŀ����_____________����װ��F��ʹ��Ba(OH)2��Һ��ʵ�����������װ��E����������0.27g��F�в�������1.97g���������ɫ����Ļ�ѧʽΪ_____________��[д��xCuCO3��yCu(OH)2����ʽ]
���𰸡� ����Cu2+ˮ�⣬��ֹ��Һ����� 8.0% NaNO2+NH4Cl![]() NaCl+N2��+2H2O Ũ���� Ӳ�ʲ�����������ɫ������ɫ��E�а�ɫ���������F����Һ����� bd ��ͣ����װ���е����屻������գ���Сʵ����� 2CuCO3��3Cu(OH)2
NaCl+N2��+2H2O Ũ���� Ӳ�ʲ�����������ɫ������ɫ��E�а�ɫ���������F����Һ����� bd ��ͣ����װ���е����屻������գ���Сʵ����� 2CuCO3��3Cu(OH)2
��������Aװ���Ʊ������ų�װ���еĿ�����B����ȫƿ��C�������ɵĵ�����װ��D�ֽ��ʽ̼��ͭ[xCuCO3yCu(OH)2]��ʢ����ˮ����ͭ��Eװ�����շֽ����ɵ�ˮ�֣�F���շֽ����ɵĶ�����̼����Gװ�����տ�����ˮ�����Ͷ�����̼����ֹ����ʵ����
(1)ͭ����ˮ�⣬����������ˮ�⣻12.5g�����к�������ͭ������Ϊ12.5g��![]() =8g��87.5mL����ˮ������Ϊ87.5g������Һ������Ϊ12.5g+87.5g=100g����������ͭ��Һ��������������Ϊ
=8g��87.5mL����ˮ������Ϊ87.5g������Һ������Ϊ12.5g+87.5g=100g����������ͭ��Һ��������������Ϊ![]() ��100%=8%���ʴ�Ϊ������Cu2+ˮ�⣬��ֹ��Һ����ǣ�8.0%��
��100%=8%���ʴ�Ϊ������Cu2+ˮ�⣬��ֹ��Һ����ǣ�8.0%��
(2)�����������ƺ��Ȼ�炙����Һ����N2���Ȼ��ƣ���ѧ����ʽΪ��NaNO2+NH4Cl![]() NaCl+N2��+2H2O���ʴ�Ϊ��NaNO2+NH4Cl
NaCl+N2��+2H2O���ʴ�Ϊ��NaNO2+NH4Cl![]() NaCl+N2��+2H2O��
NaCl+N2��+2H2O��
(3)ͨ��N2��Ŀ�����ų�װ���еĿ�����Bװ���е�װ����ѹ������ʱ��Bƿ�м�İ�ȫ����Һ��������ʹѹ���ȶ�������ȫƿ��CƿװŨ������ﵪ��������D�����ɺ�ɫ������ͭ��ˮ��ʹ��ˮ����ͭ����ɫ��������̼ʹ����ʯ��ʯ����ǣ�����Ϊ��Ӳ�ʲ�����������ɫ������ɫ��E�а�ɫ���������F����Һ����ǣ��ʴ�Ϊ��Ũ���Ӳ�ʲ�����������ɫ������ɫ��E�а�ɫ���������F����Һ����ǣ�
(4)Ba(OH)2�ܽ�ȴ���Ca(OH)2���������CO2��BaCO3��Ħ����������CaCO3���������С����������Ϊǿ�CaCO3���ܽ�Ⱥ�BaCO3�ܽ�����ʴ�Ϊ��bd��
(5)��D�з�Ӧ��ȫ����K���ٴεμ�NaNO2��Һ����N2����Ŀ������ͣ����װ���е����屻������գ���Сʵ����E�����յ���ˮ��ˮ�����ʵ���Ϊ![]() =0.015mol��F�����յ��Ƕ�����̼����̼�ᱵ��ɫ����������̼ԭ���غ�ö�����̼�����ʵ���Ϊ
=0.015mol��F�����յ��Ƕ�����̼����̼�ᱵ��ɫ����������̼ԭ���غ�ö�����̼�����ʵ���Ϊ![]() =0.01mol������ͭ�����ʵ���=(2.71g-0.27g-0.01mol��44g/mol)��80g/mol �T0.025mol����ͭ���ӡ����������Ӻ�̼������ӵ����ʵ���֮��=0.025mol��0.03mol��0.01mol=5��6��2�������仯ѧʽΪCu5(OH)6(CO3)2��д��xCuCO3��yCu(OH)2����ʽΪ��2CuCO33Cu(OH)2���ʴ�Ϊ����ͣ����װ���е����屻������գ���Сʵ����2CuCO33Cu(OH)2��
=0.01mol������ͭ�����ʵ���=(2.71g-0.27g-0.01mol��44g/mol)��80g/mol �T0.025mol����ͭ���ӡ����������Ӻ�̼������ӵ����ʵ���֮��=0.025mol��0.03mol��0.01mol=5��6��2�������仯ѧʽΪCu5(OH)6(CO3)2��д��xCuCO3��yCu(OH)2����ʽΪ��2CuCO33Cu(OH)2���ʴ�Ϊ����ͣ����װ���е����屻������գ���Сʵ����2CuCO33Cu(OH)2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����˵�ġ���ɫ��Ⱦ��ָ���ǣ�������
A.����ϩ����������
B.ʯ��Ҥ�İ�ɫ�۳�
C.ұ�����İ�ɫ�̳�
D.��ɫ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Na2CO3��NaAlO2�Ļ����Һ����μ���150 mL 1 mol L-1��HC1��Һ�������Һ��ij�������ӵ����ʵ����ı仯�����ͼ��ʾ������˵������ȷ����

A. b��c���߱�ʾ�����ӷ�Ӧ��ΪCO32-+H+= HCO3-
B. ���H+��������AlO2->CO32-> HCO3->Al(OH)3
C. M��ʱA1(OH)3����������3.9 g
D. ԭ�����Һ�У�CO32-��AlO2-�����ʵ���֮��Ϊ2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1molX�����amolY����������ɱ���ܱ������з������·�Ӧ��X��g��+aY��g��![]() bZ��g��.��Ӧ�ﵽƽ����X��ת����Ϊ25��.���ң���ͬ��ͬѹ�»���÷�Ӧǰ���������ܶ��Ƿ�Ӧ���������ܶȵ�5/6����a��b��ֵ�����ǣ� ��
bZ��g��.��Ӧ�ﵽƽ����X��ת����Ϊ25��.���ң���ͬ��ͬѹ�»���÷�Ӧǰ���������ܶ��Ƿ�Ӧ���������ܶȵ�5/6����a��b��ֵ�����ǣ� ��
A. a=1,b=2 B. a=1,b=3
C. a=2,b=3 D. a=2,b=1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������CO2��������̼������ɱ�ĺ�ѹ�ܱ������з�Ӧ��C(s)+CO2(g)![]() 2CO(g)��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ����ͼ��ʾ��
2CO(g)��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ����ͼ��ʾ��
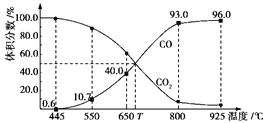
��֪�������ѹ(p��)=������ѹ(p��)���������������˵����ȷ����
A. 550��ʱ��������������壬������ ����С��ƽ�ⲻ�ƶ�
B. 650��ʱ����Ӧ��ƽ���CO2��ת����Ϊ25.0%
C. T��ʱ��������������CO2��CO��ƽ�����淴Ӧ�����ƶ�
D. 925��ʱ����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=24.0p��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ�ص�����![]() ��
��![]() ��
��![]() ��
��![]() ��������ͬ�ĵ��Ӳ�ṹ�������ƶϴ������( )
��������ͬ�ĵ��Ӳ�ṹ�������ƶϴ������( )
A. ԭ�������� ![]() B. ���Ӱ뾶��
B. ���Ӱ뾶��![]()
C. ��ԭ����![]() D. ���ԣ�
D. ���ԣ�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Ԫ�����ڱ�����������ȷ���ǣ� ��
A.��IA��Ԫ�ض��ǽ���Ԫ��
B.��VIA��Ԫ�صĵ����ڳ����¾�Ϊ����
C.�ڶ����������еĽ���Ԫ������һ ����
D.�����ڰ�����һ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Һ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ��Na2S2O3+H2SO4�TNa2SO4+SO2��+S��+H2O������ͨ�����ֻ��ǵĿ������жϷ�Ӧ�Ŀ����̶ȣ����и���ʵ�������ȳ��ֻ��ǵ��ǣ�������
ʵ�� | ��Ӧ�¶�/�� | Na2S2O3��Һ | ϡH2SO4 | ||
V/mL | c/��molL��1�� | V/mL | c/��molL��1�� | ||
A | 25 | 5 | 0.1 | 20 | 0.1 |
B | 25 | 5 | 0.2 | 10 | 0.2 |
C | 35 | 5 | 0.1 | 20 | 0.1 |
D | 35 | 5 | 0.2 | 10 | 0.2 |
A.A
B.B
C.C
D.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ٷ����ڷ�ҺΪ������ʹҩ����Ҫ��������ͷʹ�����գ�����Ҫ��ѧ�ɷֵĽṹ��ʽΪ�� ![]() �������йظ��л���������ȷ���ǣ� ��
�������йظ��л���������ȷ���ǣ� ��
A.����ʽΪC8H10NO2
B.�����ڦ����������ͬ���칹����3��
C.���л������ڦ���������
D.���л������FeCl3��Һ������ɫ��Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com