
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:

(1)已知:2Cu(s)+1/2O2(g)=Cu2O(s);△H=akJ·mol-1
C(s)+1/2O2(g)=CO(g);△H=bkJ·mol-1
Cu(s)+1/2O2(g)=CuO(s);△H=ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=_________kJ·mol-1
(2)工业上极少用方法I制取Cu2O是由于方法I反应条件不易控制,若控温不当,会降低Cu2O产率,请分析原因:________________。
(3)方法II为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为_________________________。
(4)方法III采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如下图所示:写出电极反应式并说明该装置制备Cu2O的原理___________________。

(5)在相同的密闭容器中.用以上两种方法制得的Cu2O分别进行催化分解水的实验:
![]() △H>0,水蒸气的浓度(mol/L)随时间t(min)变化如下表所示:
△H>0,水蒸气的浓度(mol/L)随时间t(min)变化如下表所示:

下列叙述正确的是_________(填字母)。
A.实验的温度:T2<T1
B.实验①前20min的平均反应速率v(O2)=7×10-5mol·L-1·min-1
C.实验②比实验①所用的Cu2O催化效率高
D.实脸①、②、③的化学平衡常数的关系:K1=K2<K3
【答案】23.(1)2c-a-b;(2)若温度不当,会生成Cu;
(3)4Cu(OH)2+N2H4![]() 2Cu2O+N2↑+6H2O;
2Cu2O+N2↑+6H2O;
(4)阴极电极反应:2H++2e-=H2↑,c(OH-)增大,通过阴离子交换膜进入阳极室,阳极电极反应:2Cu-2e-+2OH-=Cu2O+H2O,获得Cu2O;(5)CD
【解析】
试题分析:(1)根据盖斯定律,2Cu(s)+1/2O2(g)=Cu2O(s)△H=akJ·mol-1①,C(s)+1/2O2(g)=CO(g)△H=bkJ·mol-1②,Cu(s)+1/2O2(g)=CuO(s)△H=ckJ·mol-1③,根据盖斯定律2×③-①-②可得方法Ⅰ发生的反应为2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=2c-a-bkJ·mol-1。
(2)方法Ⅰ是用碳粉还原氧化铜,若温度不当,会生成Cu,降低Cu2O产率。
(3)根据题目信息:液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2,根据得失电子守恒和原子守恒配平,反应的化学方程式为:4Cu(OH)2+N2H4![]() 2Cu2O+N2↑+6H2O。
2Cu2O+N2↑+6H2O。
(4)根据电解装置图,Ti电极是阴极,溶液中的H+在阴极得电子生成氢气,则阴极电极反应为2H++2e-=H2↑,阴极c(OH-)增大,通过阴离子交换膜进入阳极室,阳极是活泼电极铜,该电极本身发生失电子的氧化反应,在碱性环境下生成Cu2O,即阳极电极反应为2Cu-2e-+2OH-=Cu2O+H2O,获得Cu2O;
(5)A.实验温度越高达到化学平衡时用的时间越短,②达到平衡用30min,而①则用了40min,所以T2>T1,A项错误;B.实验①前20min的平均反应速率v(O2)=[(0.050-0.0486)/2]÷20min=3.5×10-5molL-1min-1,B项错误;C.实验①和②化学平衡状态未改变,说明加入了催化剂,而实验②到达平衡所需的时间短,说明实验②比实验①所用的Cu2O催化效率高,C项正确;D.实验①和②化学平衡状态未改变,说明加入了催化剂,催化剂不影响化学平衡常数,则K1=K2;根据表格信息,实验③耗时更短,平衡时水蒸气的含量减少,说明平衡正向移动,平衡常数增大,即K1=K2<K3,D项正确;答案选CD。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】以物质的量为中心的相关计算,已知阿伏伽德罗常数为NA.
(1)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是___________,在相同温度和相同压强条件下,体积最大的是___________。
(2)73.0g HCl气体中含有_______个分子、________个原子、______个质子、_________个电子,标况下体积约为_______L
(3)23.75 g某+2价金属的氯化物(MCl2)中含有3.01×1023个Cl-,则MCl2的摩尔质量为________, MCl2的相对分子质量为________,M的相对原子质量为________。
(4)将0.5L1mol/L FeCl3溶液加水稀释至1L,所得溶液中氯离子的物质的量浓度是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组的同学探究以铜为电极电解电解质溶液的情况,
第一组同学以铜为电极电解饱和食盐水,探究过程如下:
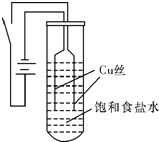
【实验Ⅰ】如图装置,电源接通后,与电池负极相连的铜丝上有大量气泡产生;与电池正极相连的铜丝由粗变细.电解开始30s内,阳极附近出现白色浑浊,然后开始出现橙黄色浑浊,此时测定溶液的pH约为10;随着沉淀量的逐渐增加,橙黄色沉淀慢慢聚集在试管底部,但溶液始终未出现蓝色。
【实验Ⅱ】将实验Ⅰ中试管底部的橙黄色沉淀取出,分装在两支小试管中,沉淀很快转变为砖红色,后续的操作及现象如下:

请回答下列问题:
(1)聚集在试管底部的橙黄色沉淀的化学式为______________.
(2)阳极的电极反应式为______________.
(3)写出实验Ⅱ中①、②的离子方程式:①__________;②__________.
(4)第二组同学将质量相等的铜片和铂片插入硫酸铜溶液中,铜片与电源正极相连铂片与电源负极相连,以电流强度1A通电10min,然后反接电源,以电流强度2A继续通电10min.画出下列表示铜电极、铂电极、电解池中产生气体的质量和电解时间的关系图,其中正确的是( )
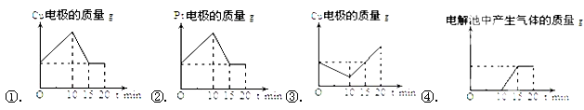
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知lg2=0.3, KSP[Cr(OH)3]=6.4×10-31。某工厂进行污水处理时,要使污水中的Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10-5时,可以认为Cr3+沉淀完全,溶液的pH至少为
A.4.4 B.5.6 C.6.7 D.8.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于生物大分子的叙述,正确的是( )
A. 蛋白质是生物大分子,生物大分子都是在核糖体上合成的
B. DNA是一切由细胞构成的生物的遗传信息载体
C. 淀粉、糖原和核糖都是生物大分子
D. 叶绿体很小,结构内不可能有蛋白质的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】俄罗斯科学家用含20个质子的钙的一种核素轰击含95个质子的镅元素,结果4次成功合成4个第115号元素的原子。这4个原子生成数微秒后衰变成第113号元素。下列有关叙述正确的是( )
A. 115号元素衰变成113号元素是化学变化
B. 核素![]() 的中子数为173
的中子数为173
C. 113号元素最高正价应为+5
D. 115号与113号元素的原子质量比为115:113
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳元素是构成细胞的最基本元素,对此最有说服力的解释是 ( )
A. 碳在细胞的各种化合物中含量最多
B. 碳在自然界中含量最为丰富
C. 在细胞的各种化合物中都含有碳
D. 碳链构成了有机物的基本骨架
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1).某化学小组利用下图装置进行实验证明氧化性:KMnO4>Cl2>Br2。
限选试剂:KBr溶液、KMnO4、浓盐酸、浓硫酸

装置a、d中盛放的试剂分别是: 、 ;实验中观察到的现象为 ;此实验装置的不足之处是 。
(2)已知:还原性HSO3>I,氧化性IO3> I2,在下图中画出向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液的过程中,析出I2的物质的量与KIO3的物质的量之间关系的曲线。
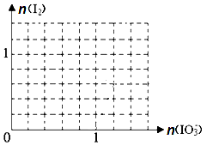
(3)已知CN-离子、SCN-离子和Cl-离子有相似之处,氰分子(CN)2和硫氰分子(SCN)2的性质与Cl2也有相似之处,且常温常压均为气体,完成下列反应方程式:
①MnO2和HSCN的浓溶液共热的化学方程式: 。
②(CN)2和NaOH溶液反应的离子方程式: 。
(4)已知H2O2是二元弱酸、请写出H2O2与Ca(OH)2溶液反应生成酸式盐的化学式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r溶液为强酸溶液,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )
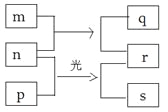
X | Y | |
Z | W |
A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com