
I、镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用 ,要使MgSO4完全转化为
沉淀,加入试剂的量应为 。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 。
(3)试剂②选用 ;写出其反应的离子方程式 。
(4)无水MgCl2在熔融状态下,通电后产生镁和氯气,该反应的化学方程式为 。
Ⅱ.关于《必修2》中提到的常见有机物,请回答下列问题:
(1)苯在常温常压下呈 态。
(2)常温常压下气态直链烷烃含碳原子数≤ 。
(3)苯和甲烷中含碳量较高的是 。
(4) 写出苯与浓硝酸、浓硫酸混合液加热反应的化学方程式(用结构简式书写) 。
(5) 写出乙醇和乙酸的酯化反应方程式 。
(每空2分,共22分)I、 (1)氢氧化钙或生石灰,过量 (2)过滤
(3)盐酸;2 H+ + Mg(OH)2=2H2O + Mg2+ (4) MgCl2(熔融) Mg + Cl2↑
Mg + Cl2↑
II.(1)液(2)4 (3)苯 (4) 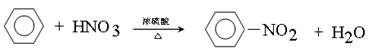
(5) CH3COOH+CH3CH2OH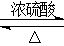 CH3COOCH2CH3 +H2O
CH3COOCH2CH3 +H2O
解析试题分析:I、(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用廉价的氢氧化钙或生石灰。要使MgSO4完全转化为沉淀,加入试剂的量应为过量的。
(2)氢氧化镁不溶于水,分离得到Mg(OH)2沉淀的方法是过滤。
(3)氢氧化镁转化为氯化镁应该用盐酸,反应的离子方程式是2H+ + Mg(OH)2=2H2O + Mg2+ 。
(4)镁是活泼的金属,应该用电解法冶炼,反应的化学方程式是 MgCl2(熔融) Mg + Cl2↑。
Mg + Cl2↑。
Ⅱ. (1)苯在常温常压下呈液态。
(2)常温常压下气态直链烷烃含碳原子数≤4,即甲烷、乙烷、丙烷和丁烷。
(3)苯和甲烷中含碳量较高的是甲苯,甲烷是含氢量最高的烃。
(4)苯与浓硝酸、浓硫酸混合液加热发生取代反应生成硝基苯,反应的化学方程式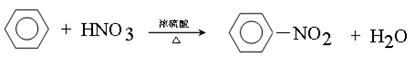 。
。
(5)乙醇和乙酸发生酯化反应生成乙酸乙酯,反应的化学方程式是CH3COOH+CH3CH2OH CH3COOCH2CH3 +H2O。
CH3COOCH2CH3 +H2O。
考点:考查海水中提取镁的有关判断、常见有机物结构、性质的有关判断以及方程式的书写
点评:该题紧扣教材基础知识,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于提高学生的应试能力,也有助于培养学生的规范答题能力,难度不大,记住并熟练应用即可。


科目:高中化学 来源: 题型:

| ||
| ||
| ||
| ||
| FeBr3 |
| FeBr3 |
查看答案和解析>>
科目:高中化学 来源:2015届云南省高一下学期期末考试化学试卷(解析版) 题型:填空题
I、镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
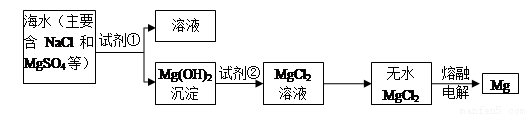
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用 ,要使MgSO4完全转化为
沉淀,加入试剂的量应为 。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 。
(3)试剂②选用 ;写出其反应的离子方程式 。
(4)无水MgCl2在熔融状态下,通电后产生镁和氯气,该反应的化学方程式为 。
Ⅱ.关于《必修2》中提到的常见有机物,请回答下列问题:
(1)苯在常温常压下呈 态。
(2)常温常压下气态直链烷烃含碳原子数≤ 。
(3)苯和甲烷中含碳量较高的是 。
(4) 写出苯与浓硝酸、浓硫酸混合液加热反应的化学方程式(用结构简式书写) 。
(5) 写出乙醇和乙酸的酯化反应方程式 。
查看答案和解析>>
科目:高中化学 来源:09-10年北京市朝阳区高一下学期期末考试化学卷 题型:填空题
(10分)海水中化学资源的综合开发利用已受到各国的高度重视。Br2和Mg等两种单质都可以从海水中提取,下图为提取它们的步骤:

请回答:
I.从海水中提取的溴占世界年产量的1/3,主要方法就是上述流程中的空气吹出法。
(1)制取Br2时,第一次通入Cl2发生反应的离子方程式是__________________。
(2)吸收塔中反应的离子方程式是________________________________________。
由(1)、(2)可知,SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
__________________。( 用“”表示)
II.镁及其合金是用途很广泛的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的。
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用___________(写化学式)。
(2)加入试剂②后反应泊离子方程式是_________________________________。
(3)步骤①包括加热、蒸发、冷却、结晶、_________。
(4)通电时无水MgCl2在熔融状态下反应的化学方程式是
___________________________________________________。
III.上述流程在生产溴和镁的同时还可以制得其他化工物质,比如制备耐火材料氧化镁和盐酸。生产方法是:
①将氯化镁晶体(MgCl2·6H2O)加热到523OC以上,该晶体可以分解得到耐火材料氧化镁和两种气态化合物,其中一种气体常温下为无色液体。
②将两种气体冷却到室温,再根据需要,加入不同量的水,就可得到不同浓度的盐酸。
(1)MgCl2·6H2O在523OC以上分解的化学方程式是_____________________________。
(2)现用1mol MgCl2·6H2O分解所得的非固体产物来制取密度为1.19g/cm3的盐酸溶液168mL,需加水__________g(精确到0.1),该盐酸中溶质的物质的量浓度是____________mol/L(精确到0.1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
I、镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
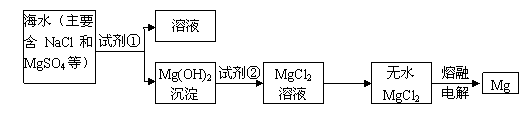
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用 ,要使MgSO4完全转化为
沉淀,加入试剂的量应为 。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 。
(3)试剂②选用 ;写出其反应的离子方程式 。
(4)无水MgCl2在熔融状态下,通电后产生镁和氯气,该反应的化学方程式为 。
II.关于《必修2》中提到的常见有机物,请回答下列问题:
(1)苯在常温常压下呈 态。
(2)常温常压下气态直链烷烃含碳原子数≤ 。
(3)苯和甲烷中含碳量较高的是 。
(4) 写出苯与浓硝酸、浓硫酸混合液加热反应的化学方程式(用结构简式书写) 。
(5) 写出乙醇和乙酸的酯化反应方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com