
| A. | 元素的相对原子质量递增,量变引起质变 | |
| B. | 元素原子核外电子排布呈周期性变化 | |
| C. | 元素的原子半径由大到小变化 | |
| D. | 元素的化合价呈周期性变化 |
分析 根据随原子序数的递增,原子的结构呈现周期性的变化而引起元素的性质的周期性变化来解答.
解答 解:A、因随原子的相对原子质量的递增,元素发生变化,但不能说明周期性变化,故A错误;
B、因原子的核外电子排布中电子层数和最外层电子数都随原子序数的递增而呈现周期性变化,则引起元素的性质的周期性变化,故B正确;
C、因元素的原子半径是元素的性质,不能解释元素性质的周期性变化,故C错误;
D、因元素的化合价属于元素的性质,则不能解释元素性质的周期性变化,故D错误;
故选:B.
点评 本题考查元素周期律的实质,明确原子的结构与性质的关系、元素的性质有哪些是解答的关键,并注意不能用元素本身的性质来解释元素性质的周期性变化.


科目:高中化学 来源: 题型:解答题
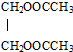 (过程中无机产物已忽略)
(过程中无机产物已忽略) .
.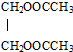 的反应方程式CH3COOH+HOCH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$
的反应方程式CH3COOH+HOCH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$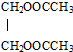 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
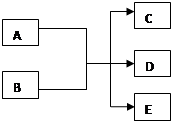 在一定条件下,某些化学反应可以如图框架表示(未注明反应条件),根据要求回答下列问题:
在一定条件下,某些化学反应可以如图框架表示(未注明反应条件),根据要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第3列所含元素种类最多 | B. | 第1列元素中全为金属元素 | ||
| C. | 第15的气态氢化物为RH3 | D. | 第17列元素的第一种元素无含氧酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
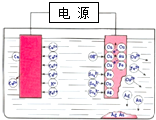
| A. | 右边电极材料为精铜 | |
| B. | 电解质溶液可选择CuSO4溶液 | |
| C. | 随着电解的进行,溶液中Cu2+浓度逐渐增加 | |
| D. | 阳极质量的减小量等于阴极质量的增加量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠溶液 | B. | 氯化铁溶液 | C. | 硝酸钡溶液 | D. | 硝酸钙溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内压强不随时间变化 | B. | V正(X)=2V逆(Z) | ||
| C. | 容器内X、Y、Z的浓度相等 | D. | 容器内气体密度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 | |
| B. | 常用的二次电池铅蓄电池充电时电池正极与电源负极相接 | |
| C. | 用铂电极电解CuSO4溶液,当Cu2+浓度降低至原来一半时,加入CuO使溶液恢复到原来浓度和质量 | |
| D. | 在轮船船壳吃水线下焊上铜块可避免船体遭受腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com