
| A. | Cl2能与大多数金属反应 | |
| B. | N2是大气中的主要成分之一,雷雨时可直接转化为NO2 | |
| C. | 硫是一种黄色的能溶于水的晶体,既有氧化性又有还原性 | |
| D. | 硅是应用广泛的半导体材料,常温下化学性质活泼 |
分析 A、氯气具有强氧化性,能与金属活动性顺序表中大多数金属反应;
B、放电时,氮气和氧气反应生成NO;
C.硫是淡黄色固体,不溶于水;
D、硅的化学性质不活泼.
解答 解:A、氯气具有强氧化性,能与金属活动性顺序表中大多数金属反应生成氯化物,和变价金属反应时使其氧化为最高价态,故A正确;
B、放电时,氮气和氧气反应生成NO,NO不稳定,继续被氧气氧化生成NO2,故B错误;
C.硫是淡黄色固体,不溶于水,微溶于酒精,易溶于二硫化碳,故C错误;
D、硅的导电性介于导体和绝缘体之间,是应用广泛的半导体材料,硅的化学性质不活泼,故D错误;
故选A.
点评 本题考查非金属元素性质,侧重考查元素化合物知识,注意氯气的强氧化性、硫单质的物理性质,题目难度不大.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
| A. | 对因胃酸过多而导致胃部严重溃疡的病人不可使用含有碳酸氢钠的药物治疗 | |
| B. | 淀粉、纤维素水解的最终产物都是葡萄糖 | |
| C. | 误食了重金属离子,应立即喝大量牛奶来缓解毒性 | |
| D. | R表示非处方药,OTC表示处方药 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
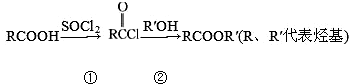 ,①②两步的产率均可达到90%以上,而RCOOH直接转化为RCOOR′产率在 60%左右,则下列说法不正确的是( )
,①②两步的产率均可达到90%以上,而RCOOH直接转化为RCOOR′产率在 60%左右,则下列说法不正确的是( )| A. | ①②两步均为取代反应 | |
| B. | ①②总产率比羧酸直接与醇反应产率高 | |
| C. | SOCl2若与足量羧酸反应产物除了 外,还有硫酸 外,还有硫酸 | |
| D. | SOCl2可以和水反应,故①反应不能用醋酸水溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -80 kJ/mol | B. | -90 kJ/mol | C. | -60 kJ/mol | D. | -70 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能加大反应速率、促进平衡向三氧化硫的方向移动 | |
| B. | 能提高二氧化硫的利用率、使原料不被浪费 | |
| C. | 能提高三氧化硫的平衡浓度 | |
| D. | 加大正逆反应速率,缩短达到平衡的时间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷(丙烯):通入溴水 | |
| B. | 乙烷(乙烯):通入酸性高锰酸钾溶液 | |
| C. | CO2(SO2):气体通过盛氢氧化钠溶液的洗气瓶 | |
| D. | 乙醇(乙酸):加足量浓硫酸,蒸馏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com