
| A. | 向Fe、FeO和Fe2O3的混合物中加入过量的盐酸 | |
| B. | 等物质的量的 NaHCO3溶液与 Na2O2固体 | |
| C. | 等物质的量浓度、等体积的(NH4)2SO4与 BaC12溶液 | |
| D. | 在NaBr溶液中通入过量氯气 |
分析 A.Fe、FeO和Fe2O3的混合物中加入过量盐酸生成氯化铁,氯化铁会水解得到氢氧化铁和盐酸,盐酸挥发,氢氧化铁分解最终得到氧化铁;
B.等物质的量的NaHCO3与Na2O2固体混合,发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,过氧化钠再与二氧化碳、水反应;
C.等物质的量的浓度、等体积的(NH4)2SO4与BaCl2溶液,反应生成硫酸钡和氯化铵,氯化铵分解生成氨气和HCl;
D.在NaBr溶液中通入过量Cl2,反应生成NaCl、溴,溴易挥发.
解答 解:A.Fe、FeO和Fe2O3的混合物中加入过量盐酸生成氯化铁,氯化铁会水解得到氢氧化铁和盐酸,盐酸挥发,灼烧氢氧化铁分解最终得到氧化铁,为纯净物,故A错误;
B.等物质的量的NaHCO3与Na2O2固体混合,发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,过氧化钠再与二氧化碳、水反应,蒸干灼烧后的固体为碳酸钠和NaOH,为混合物,故B正确;
C.等物质的量的浓度、等体积的(NH4)2SO4与BaCl2溶液,反应生成硫酸钡和氯化铵,氯化铵分解生成氨气和HCl,蒸干灼烧后的固体为硫酸钡,为纯净物,故C错误;
D.在NaBr溶液中通入过量Cl2,反应生成NaCl、溴,溴易挥发,蒸干灼烧后的固体为NaCl,为纯净物,故D错误;
故选B.
点评 本题考查物质的性质,明确发生的化学反应及物质的性质是解答本题的关键,题目难度中等.


 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
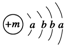 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
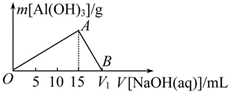 向20mL某浓度的AlCl3溶液中滴加2mol•L-1的NaOH溶液时,所得沉淀的质量与加入NaOH溶液的体积之间的关系如图所示:
向20mL某浓度的AlCl3溶液中滴加2mol•L-1的NaOH溶液时,所得沉淀的质量与加入NaOH溶液的体积之间的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
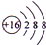 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol MgCl2中含有的离子数为3NA | |
| B. | 标况下3.36LCCl4中所含碳原子数约为0.15×6.02×1023 | |
| C. | 标准状况下,22.4L氦气与22.4L氯气所含原子数均为2NA | |
| D. | 标准状况下,1molCl2在反应中一定得到2NA电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别加入1mol/L的盐酸溶液,看有无气泡产生 | |
| B. | 分别取样配成溶液,滴加Ca(OH)2溶液,观察有无白色沉淀 | |
| C. | 用铂丝粘取固体在酒精灯火焰上灼烧,观察火焰的颜色,NaHCO3的焰色为紫色 | |
| D. | 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com