
��ͼ��ʵ�����Ʊ�����������һϵ�����ʵ���װ��(�гּ�������������)��
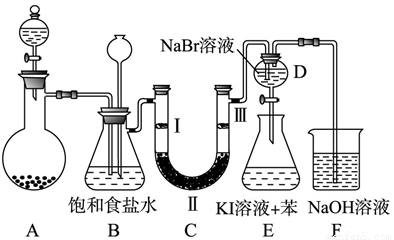
��1���Ʊ�����ѡ�õ�ҩƷΪ����������̺�Ũ���ᣬ����صĻ�ѧ��Ӧ����ʽΪ�� ��
װ��B�б���ʳ��ˮ�������� ��ͬʱװ��B���ǰ�ȫƿ�����ʵ�����ʱC���Ƿ�����������д����������ʱB�е����� ��
��2��װ��C��ʵ��Ŀ������֤�����Ƿ����Ư���ԣ�Ϊ��C�Т����η��� ��
| a | b | c | d |
�� | �������ɫ���� | �������ɫ���� | ʪ�����ɫ���� | ʪ�����ɫ���� |
�� | ��ʯ�� | �轺 | Ũ���� | ��ˮ�Ȼ��� |
�� | ʪ�����ɫ���� | ʪ�����ɫ���� | �������ɫ���� | �������ɫ���� |
��3�����װ��D��E��Ŀ���DZȽ��ȡ��塢�ⵥ�ʵ�������ǿ��������D�л���ͨ����������ʱ�����Կ�����ɫ��Һ��Ϊ ɫ����������װ��D��������Һ����װ��E�У����۲쵽�������� ��
��4��װ��F����������NaOH��Һ�������ȣ���д����Ӧ�Ļ�ѧ����ʽ�� ��
��1��MnO2��4HCl(Ũ)  MnCl2��Cl2����2H2O��2�֣� ��ȥCl2�е�HCl��2�֣� B�г���©����Һ���������γ�ˮ����2�֣�
MnCl2��Cl2����2H2O��2�֣� ��ȥCl2�е�HCl��2�֣� B�г���©����Һ���������γ�ˮ����2�֣�
��2��d��2�֣�
��3���ƣ�2�֣� E����Һ��Ϊ���㣬�ϲ�(����)Ϊ�Ϻ�ɫ��2�֣�
��4��2NaOH��Cl2===NaCl��NaClO��H2O��2�֣�
��������
�����������1������������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�ˮ����������ѧ����ʽΪMnO2��4HCl(Ũ)  MnCl2��Cl2����2H2O����ΪŨ�����ӷ������������к���������HCl����˱���ʳ��ˮ�������dz�ȥ�����е�HCl����װ��C������������Bװ�õ�ѹǿ��������B�г���©����Һ���������γ�һ��ˮ����
MnCl2��Cl2����2H2O����ΪŨ�����ӷ������������к���������HCl����˱���ʳ��ˮ�������dz�ȥ�����е�HCl����װ��C������������Bװ�õ�ѹǿ��������B�г���©����Һ���������γ�һ��ˮ����
��2����������ʹ�������ɫ������ɫ������ʹʪ�����ɫ������ɫ��������װ��B�г�������������ˮ����������I����ʪ�����ɫ������II���ż�ʯ�ң���������������III���Ÿ������ɫ��������I���Ÿ������ɫ��������Ϊ�����к���ˮ����������ʵ��������III��������ͬ�����ܼ��������Ƿ����Ư���ԣ����Դ�ѡd��
��3���������廯�Ʒ�Ӧ�����嵥�ʣ�����װ��D����Һ��ɫ��ƣ�װ��D��������Һ����װ��E�У���ΪD��������ڣ�����KI�����û���Ӧ���еⵥ�����ɣ����ڱ��е��ܽ�ȴ�����ˮ�е��ܽ�ȣ��ұ����ܶ�С��ˮ������ˮ�����ܣ�������Һ�ֲ㣬�ϲ���ҺΪ�Ϻ�ɫ��
��4�����������������������Һ���գ��������������Ʒ�Ӧ�����Ȼ��ơ��������ơ�ˮ����ѧ����ʽΪ2NaOH��Cl2===NaCl��NaClO��H2O��
���㣺������������ȡ�����ӡ�β���Ĵ�����±��֮����û���Ӧ��������ж�


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
��5�֣���һ����ϵ���ĵ�λ�����ǿ��Եó������ļ��㹫ʽ���磺��Ħ�������ĵ�λ��g��mol��1 ���ɵó�����Ӧ������������ĸӦ�������ʵ��������Ħ�������ļ��㹫ʽΪ M �� m / n���Դ����ƣ����ʵ���Ũ�ȵ�λ�� ������㹫ʽc �� ��
�������������ʵ����Ĺ�ϵ�Ƴ�����ӵ������Ĺ�ʽNA �� ��
����Ħ������ĵ�λ�� ������㹫ʽ��Vm �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
�ڱ�״���£���CO��CO2��ɵĻ������8.96 L������Ϊ16g����˻������CO��CO2���ʵ���֮���� ��C��Oԭ�Ӹ������� ��������������ܶ��� ����û����������̼ԭ������ͬ��CH4������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й������ӵļ���˵����ȷ����
A����ij��Һ�е����������ᣬ��۲쵽��ɫ��ζ���������������ʹ����ʯ��ˮ����ǣ���֤����Һ�бض���CO32-
B����ij��ɫ��Һ�м���BaCl2��Һ���а�ɫ�������֣��ټ���ϡ���ᣬ��������ʧ����֤����Һһ������SO42-
C����ij��ɫ��Һ�м�������ϡ����������Һ����ʪ��ĺ�ɫʯ����ֽ�����Թܿڣ�����ֽ����������˵������Һ����NH4+
D��������ɫ���ܲ����ܹ��۲쵽��ɫ���棬��һ���м�Ԫ�أ�һ����������Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������ڵ���ʲ��ܵ������
�����ڵ�NaCl �� KNO3��Һ ��Cu �ܾƾ� ��KCl����
A���� B���٢� C���٢ڢ� D���٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ�����и�һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ǰ���NH2OH����һ�ֻ�ԭ�����ܽ�ijЩ��������ԭ������25.00ml0.049mol/L�ǰ���������Һ��������������Һ��ȫ��Ӧ�����ɵ�Fe2+ǡ����24.50ml0.020mol/LKMnO4������Һ��ȫ���á���֪��2KMnO4+10FeSO4=5Fe2��SO4��3+K2SO4+2MnSO4+8H2O������������Ӧ���ǰ�������������
A��N2 B��N2O C��NO D��NO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ�����и�һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
"NaCl+CO2+NH3+H2O=NaHCO3��+NH4Cl"��������"�����Ƽ"����Ҫ��Ӧ��������4λͬѧ�Ը÷�Ӧ�漰���й�֪ʶ�����IJ��ּ��⡣���в���ȷ����
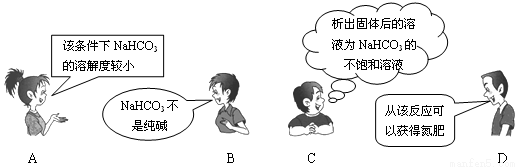
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ�����и�һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ƿ�ϲ�����ǵ���
A���̶��� B���������
C���¶� D����Һ�����ʵ���Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�ʡ�߶���ѧ�����л�ѧ�������Ծ��������棩 ���ͣ������
��7�֣���1����֪��2H2(g) + O2(g) == 2H2O(g)����H= �C483��6 kJ�� , H2(g) + 1/2O2(g) == H2O(l)�ġ�H=�C285��8 kJ��
, H2(g) + 1/2O2(g) == H2O(l)�ġ�H=�C285��8 kJ�� ,�ɴ˿�֪���ڵ���������18gҺ̬ˮ������_____ kJ��������
,�ɴ˿�֪���ڵ���������18gҺ̬ˮ������_____ kJ��������
��2����3�֣���ҵ��������һ����Ҫ��Ӧ�ǣ�CO(g)+ H2O(g) == CO2(g) + H2(g)
��֪25��ʱ��
C(ʯī) +O2 (g) == CO2(g) ��H1 ����394 kJ��mol-1
C(ʯī) +1��2O2 (g) == CO (g) ��H2 ����111 kJ��mol-1
H2(g) +1��2O2 (g)== H2O(g) ��H3����242kJ��mol-1���Լ���25��ʱCO(g)+ H2O(g) == CO2(g) + H2(g)�ķ�Ӧ��_______ kJ��mol-1
��3����25�桢101KPaʱ��____________________________ʱ���ų��������������÷�Ӧ��ȼ���ȡ���25�桢101KPaʱ��1g�Ҵ���ȫȼ������CO2��Һ̬ˮʱ����29��713kJ�����ܱ�ʾ�Ҵ�ȼ���ȵ��Ȼ�ѧ����ʽΪ__________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com