
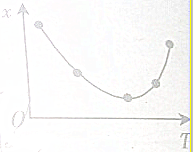
 在某恒容密闭容器中通入一定量的二氧化氮,发生反应:2NO2(g)?N2O4(g),测定体系中x随着反应温度(T)变化的关系如图所示,下列关于x说法正确的是( )
在某恒容密闭容器中通入一定量的二氧化氮,发生反应:2NO2(g)?N2O4(g),测定体系中x随着反应温度(T)变化的关系如图所示,下列关于x说法正确的是( )| A、表示二氧化氮的转化率 |
| B、表示二氧化氮的体积分数 |
| C、表示该反应的平衡常数 |
| D、表示该密闭容器混合气体的密度 |


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学生欲用已知物质的量浓度为0.1000mol/L的NaOH溶液来测定未知物质的量浓度的盐酸,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度为0.1000mol/L的NaOH溶液来测定未知物质的量浓度的盐酸,选择酚酞作指示剂.请填写下列空白:| 实验 编号 | NaOH溶液的 浓度/mol?L-1 | 滴定完成时,溶液滴入的体积/mL aOH | 待测盐的体积/mL酸 |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
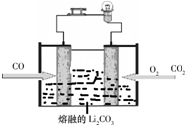 定”).
定”).查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作步骤 | 实验现象 | 实验结论 |
| 取少量滴有酚酞试液的试样于小试管中,滴加足量的 | 溶液由红色褪为无色 且有白色沉淀产生 | 猜想②正确 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取少量试样于小试管中,滴加适量的 | 猜想②正确 有关化学方程式 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 -OH和
-OH和 CH2OHE.NH2CH2COOH与NH2CH(CH3)COOHF.CH3CHO与CH2=CHCHO.
CH2OHE.NH2CH2COOH与NH2CH(CH3)COOHF.CH3CHO与CH2=CHCHO.查看答案和解析>>
科目:高中化学 来源: 题型:
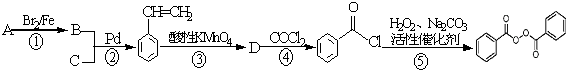
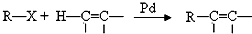
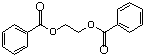 的流程,无机物任选,注明反应条件.
的流程,无机物任选,注明反应条件.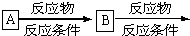
查看答案和解析>>
科目:高中化学 来源: 题型:
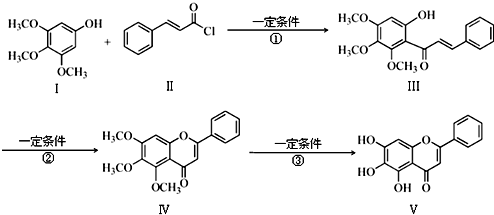
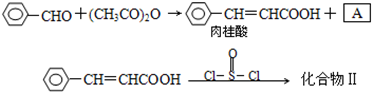
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com