
| A. | 向含4molFeBr2 溶液中通入 3molCl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| B. | 用食醋除去水壶内的水垢:CaCO3+2H+=Ca2++CO2↑+H2O | |
| C. | KHCO3与足量澄清石灰水反应:HCO3-+Ca2++OH-=CaCO3+H2O | |
| D. | 在强碱性溶液中,次氯酸钠将Mn2+氧化成MnO2:Mn2++ClO-+H2O=MnO2↓+Cl-+2H+ |
分析 A.4molFeBr2完全反应消耗6mol氯气,氯气不足,亚铁离子优先反应,剩余的氯气再氧化溴离子;
B.醋酸为弱酸,离子方程式中醋酸不能拆开;
C.澄清石灰水足量,离子方程式按照碳酸氢钾的化学式组成书写;
D.反应环境为强碱性溶液,反应产物中不能生成氢离子.
解答 解:A.向含4molFeBr2 溶液中通入3molCl2,4mol亚铁离子优先反应消耗2mol氯气,剩余的1mol氯气能够氧化2mol溴离子,参与反应的亚铁离子与溴离子的物质的量之比为2:1,正确的离子方程式为:4Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-,故A错误;
B.碳酸钙和醋酸都不能拆开,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故B错误;
C.KHCO3与足量澄清石灰水反应生成氢氧化钾、碳酸钙沉淀和水,反应的离子方程式为:HCO3-+Ca2++OH-=CaCO3+H2O,故C正确;
D.在强碱性溶液中,次氯酸钠将Mn2+氧化成MnO2,正确的离子方程式为:Mn2++2OH-+ClO-=MnO2↓+Cl-+H2O,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,题目难度不大,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:填空题
 ③金刚石 ④35Cl ⑤
③金刚石 ④35Cl ⑤
 ⑦
⑦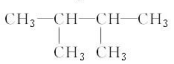 ⑧氯气 ⑨石墨 ⑩37Cl
⑧氯气 ⑨石墨 ⑩37Cl
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8g Na2O2 与足量的 CO2充分反应转移的电子数为 0.2NA | |
| B. | 常温常压下,23gNO2和N2O4混合气体中含氧原子数为 NA | |
| C. | l04g 苯乙烯(C6H5‐CH=CH2 )中含有 8NA的碳氢键和 4NA的碳碳双键 | |
| D. | 将1mol氯气通入足量水中,则 N(HClO)+N(Cl-)+N(ClO-)=2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8、7 | B. | 9、4 | C. | 4、9 | D. | 6、10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 将漫射光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上,如图.下列现象描述正确的是( )
将漫射光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上,如图.下列现象描述正确的是( )| A. | 只有①② | B. | 只有①③ | C. | 只有①②③ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解熔融氯化钠:2Cl-+2H2O═Cl2↑+H2↑+2OH- | |
| B. | 碳酸氢铵溶液中加入足量氢氧化钡溶液:NH4++HCO3-+2OH-═CO32-+NH3•H2O+H2O | |
| C. | Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 | |
| D. | NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2--+6H+═2Mn2++5NO3-+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示装置,可观察到电流计指针偏转,M棒变粗,N棒变细.表所列M、N、P物质中,可以组合成该装置的是( )
如图所示装置,可观察到电流计指针偏转,M棒变粗,N棒变细.表所列M、N、P物质中,可以组合成该装置的是( )| A | B | C | D | |
| M | 锌 | 铜 | 银 | 锌 |
| N | 铜 | 铁 | 锌 | 铁 |
| P | 稀H2SO4 | 稀盐酸 | AgNO3溶液 | Fe(NO3)3溶液 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 阳极与阴极上的产物的物质的量之比为1:1 | |
| B. | 电解过程中溶质的浓度不变 | |
| C. | 电解过程中b极质量减少 | |
| D. | a是阴极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com