

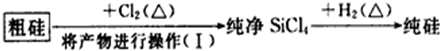
| ���� | Si | SiCl4 |
| �е�/�� | 2355 | 57.6 |
���� MgΪ���ý������ڿ����е�ȼ���Ժ�O2��CO2��H2O��Ӧ���ڹ�ҵ������þ��ȡ�裺���ž�װ���еĿ�����ʵ����Ӧͨ������X��Ϊ��������X��ϡ�����Ƶã�������ɣ�1����Ϣ��֪����п��ϡ�����Ƶõ������ſ�װ���еĿ����������Ϳ����Ļ������ȼ�ջᷢ����ը�����Է�Ӧ��ʼǰӦ����ͨ�����ž�װ���еĿ�����XΪ������ͨ��Ũ������и������Ӧ��ʼ�����߾ƾ��Ʒ�Ӧ�ܼ������У�Mg��SiO2��Ӧ�Ƿ��ȷ�Ӧ����Ӧ��������ȴ������ʱ������Ӧ��Ļ�����м���ϡ���ᷢ��Mg2Si+4HCl�T2MgCl2+SiH4����SiH4+2O2�TSiO2+2H2O��
��1��Mg������CO2��N2������ѧ��Ӧ��Mg���������ܷ�����Ӧ���Ʊ�������ϡ�����п����ͨ��Ũ������
��2������������ȼ�ջᷢ����ը��Mg��SiO2��Ӧ�������Ǽ��ȣ���Ӧ�������ɷ�Ӧ����ά�֣�
��3��Mg2Si������Ѹ�ٷ�Ӧ����SiH4�����飩��SiH4�ڳ�������һ�ֲ��ȶ�������ȼ�����壻
��4�����������ʣ���SiO2�ȣ����ƴֹ裬Si��������Ӧ�����������Ȼ��裬SiCl4�е�ͣ�57.6����ʹSiCl4��װ��B���ݳ���H2��ֻ�ϣ�Ӧ��ʹ���Ȼ���ת��Ϊ���壬����������ԭ���Ȼ���õ�������Si��
��� �⣺��1��Mg������CO2��N2������ѧ��Ӧ��Mg���������ܷ�����Ӧ����˿���������Ϊ��������ѡ�õ�ҩƷΪϡ�����п��������Ũ����������CΪŨ���
�ʴ�Ϊ���٣��ޣ��ڣ�
��2��װ�����п����������������ſ�װ���еĿ����������Ϳ����Ļ������ȼ�ջᷢ����ը�����Է�Ӧ��ʼǰӦ����ͨ�����ž�װ���еĿ�����Mg��SiO2��Ӧ�������Ǽ��ȣ�ֹͣ���Ⱥ�Ӧ�������ɷ�Ӧ�ų�������ά�֣�
�ʴ�Ϊ����ֹ����������H2�������ϱ�ը��Mg��SiO2�ķ�Ӧ�Ƿ��ȷ�Ӧ��
��3��Mg2Si������Ѹ�ٷ�Ӧ����SiH4�����飩���䷴Ӧ�ķ���ʽΪ��Mg2Si+4HCI=2MgCl2+SiH4����SiH4��������һ�ֲ��ȶ�������ȼ�����壬��Ӧ�ķ���ʽΪSiH4+2O2�TSiO2+2H2O����������Ӧ��Ļ�����м���ϡ���ᣬ�ɹ۲쵽�����Ļ��ǣ�
�ʴ�Ϊ��Mg2Si+4HCl=2MgCl2+SiH4����SiH4+2O2�TSiO2+2H2O��
��4�����������ʣ���SiO2�ȣ����ƴֹ裬Si��������Ӧ�����������Ȼ��裬��Ӧ�ķ���ʽΪ��Si+2Cl2$\frac{\underline{\;\;��\;\;}}{\;}$SiCl4������������ԭ���Ȼ���õ�������Si���䷴Ӧ�ķ���ʽΪ��SiCl4+2H2$\frac{\underline{\;\;��\;\;}}{\;}$Si+4HCl��SiCl4�е�ͣ�57.6����ʹSiCl4��װ�����ݳ���H2��ֻ�ϣ�Ӧ��ʹ���Ȼ���ת��Ϊ���壬���Զ��������Ȼ����װ�ý������õ����������Ȼ��裬
�ʴ�Ϊ������Si+2Cl2$\frac{\underline{\;\;��\;\;}}{\;}$SiCl4��SiCl4+2H2$\frac{\underline{\;\;��\;\;}}{\;}$Si+4HCl��
���� ���⿼�������ʵ��Ʊ�ԭ����װ��ѡ��ʵ�鲽�����Ʒ����жϣ��������ʵ������ǽ���ؼ�����Ŀ�Ѷ��еȣ������ڿ���ѧ����ʵ��̽��������


 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��ͭ������ۻ�Ͼ��ȼ�������ȡCuS | |
| B�� | ��ͭ˿����Ũ�����в����ȣ���Ӧ���ټ�ˮ�Թ۲�CuSO4��Һ����ɫ | |
| C�� | ��CuSO4��Һ�м��������NaOH��Һ������ϴ�Ӳ��ռ����������������ȡCuO | |
| D�� | �������Һ�м�������ϡ�����ȣ��ټ���������Cu��OH��2�����ȣ�����ש��ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | NaOH�������ʱ����� | B�� | ʢ�ű�����ĵζ����ü�Һ��ϴ | ||
| C�� | �÷�̪��ָʾ�� | D�� | ����NaOH�к���Na2O���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
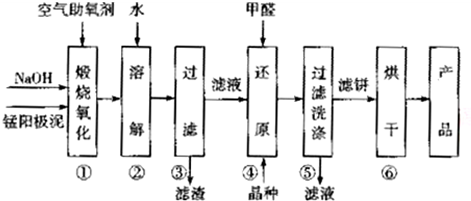
| ���� | MnSO4 | Mn��OH��2 | MnO2 |
| �ܽ��Ի�Ksp | ���� | 1.9��10-13 | ���� |
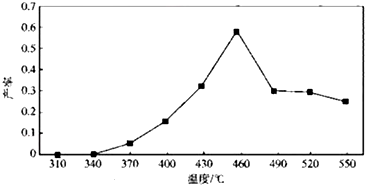
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
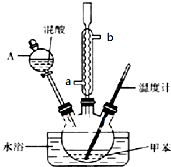 ijʵ��С������ͼ��ʾ��װ���Ʊ�һ�����ױ������������ױ��Ͷ������ױ�����
ijʵ��С������ͼ��ʾ��װ���Ʊ�һ�����ױ������������ױ��Ͷ������ױ�����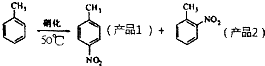
| �ܶ�g•cm-3 | �е�/�� | �ܽ��� | |
| �ױ� | 0.866 | 110.6 | ������ˮ�������������ױ� |
| ��Ʒ1 | 1.286 | 237.7 | ������ˮ��������Һ���� |
| ��Ʒ2 | 1.162 | 222 | ������ˮ��������Һ���� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
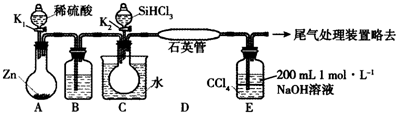
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
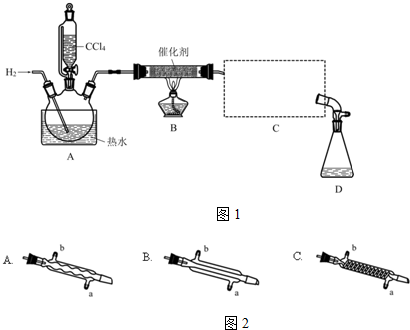
| ���� | ��Է������� | �ܶ�/��g•mL-1�� | �е�/�� | ˮ���ܽ��� |
| CHCl3 | 119.5 | 1.50 | 61.3 | ���� |
| CCl4 | 154 | 1.59 | 76.7 | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
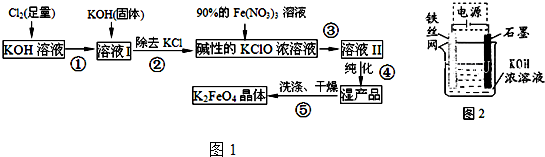
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
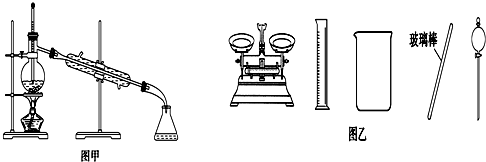
| A�� | ��δ֪Һ����ζʱ��Ӧ�ý��Լ�ƿ�ھ���ڱ�ԶһЩ�����������ȶ� | |
| B�� | ���ⵥ�ʴӵ��CCl4��Һ�з������������ͼ����ʾʵ��װ�� | |
| C�� | ������ƿ���ƺ�һ��Ũ�ȵ�ij��Һ������ƿ����������ƿ�����ϱ�ǩ | |
| D�� | ����500 mL 0.4 mol•L-1NaCl��Һ����Ҫ��������ͼ����ʾ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com