
���� ��1���Ʊ�������������ķ�������25ml��ˮ����μ���1��2mL FeCl3������Һ�������������Һ�ʺ��ɫ��ֹͣ���ȣ�
��2��ֻ�н�����ж����ЧӦ��������֤����IJ������Ʊ�Fe��OH��3�����ԭ�������������ˮ�⣬�Ȼ���ˮ�����������������壻
��3������ĵ�Ӿʵ��֤���˽��彺���Ǵ���ģ������м�������Ե��Ρ����ȡ������������ʹ����۳���
��� �⣺��1����ͬѧ��1mol•L-�Ȼ�����Һ�м���������NaOH��Һ���ᷢ�����ֽⷴӦ���ɺ��ɫ��������ͬѧֱ�Ӽ��ȱ���FeCl3��Һ����������ˮ�����ɺ��ɫ�������Ʊ�������������ķ�������25ml��ˮ����μ���1��2mL FeCl3������Һ�������������Һ�ʺ��ɫ��ֹͣ���ȣ�
�ʴ�Ϊ����ͬѧ��
��2��������ж����ЧӦ��������ͨ������ʱ���Ӳ���۲쵽һ�������ġ�ͨ·�����Ȼ���ˮ�����������������壬��ѧ����ʽ��FeCl3+3H2O����ˮ��?Fe��OH��3�����壩+3HCl��
�ʴ�Ϊ���ü����������Һ�����������ԵĹ�·����˵����Fe��OH��3�������ɣ�FeCl3+3H2O����ˮ��?Fe��OH��3�����壩+3HCl��
��3��������е�Ӿ���ʣ���Ӿʵ��֤���˽��彺�����㣬�������ƶ���˵��Fe��OH��3���������磬������о۳������ʣ������м�������Ե��Ρ����ȡ������������ʹ����۳���
�ʴ�Ϊ�������к��ɫ�������ɣ�
���� ���⿼��Fe��OH��3������Ʊ�֪ʶ��ע��������������ľ۳��Լ��������ܽ�ԭ���ǽ����Ĺؼ���ע�⽺���е�Ӿ���۳������ʣ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 | B�� | 2 | C�� | 3 | D�� | 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ũ�ȵ���Һ�е���ϡ���ᣮ�ų�����Ŀ���Na2C03��NaC03 | |
| B�� | ���ȶ���Na2C03��NaHC03 | |
| C�� | ����ʱˮ����Na2C03��NaHC03 | |
| D�� | ��Է�������Na2C03��NaHC03 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
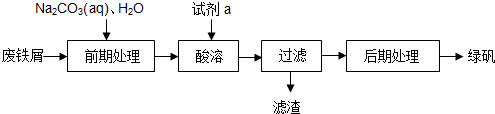
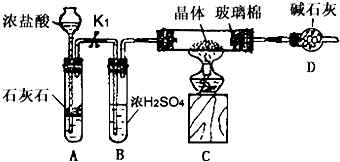
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���е����ӷ�Ӧ����ʽ�ǣ�Na++NH3+CO2+H2O=NaHCO3��+NH4+ | |
| B�� | ���е����ӷ�Ӧ����ʽ�ǣ�2Na++CO32-+H2O+CO2=2NaHCO3�� | |
| C�� | �����仯˵����ͬ�¶����ܽ��Na2CO3��NaHCO3��NaCl | |
| D�� | ��CaCl2��Һ�м���ŨBa��OH��2��Һ��Ҳ���������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com