
| a |
| a+16×3 |
| 32 |
| 2 |
| m |
| M |
| n |
| V |
| a |
| a+16×3 |
| 32 |
| 2 |
| 17g |
| 34g/mol |
| 1mol |
| 0.5L |


科目:高中化学 来源: 题型:
| A、38Sr是第3周期ⅡA族元素 |
| B、Sr的离子半径比Ar的原子半径大 |
| C、Sr的碳酸盐受热会分解 |
| D、Sr的氧化物对应水化物碱性比Rb的氧化物对应水化物碱性弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 |
| B、2NO(g)+2CO(g)═N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H>0 |
| C、加热0.1mol?L-1 Na2CO3溶液,CO32-的水解程度和溶液的pH均增大 |
| D、对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
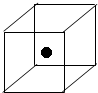 通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),下表为一些常见化学键键能值.
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),下表为一些常见化学键键能值.| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
查看答案和解析>>
科目:高中化学 来源: 题型:

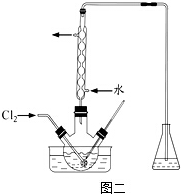
查看答案和解析>>
科目:高中化学 来源: 题型:
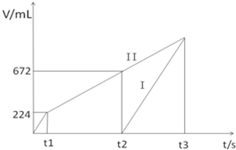
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
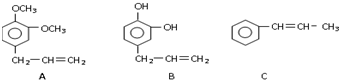
| 氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、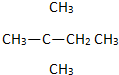 |
| B、CH3 CH2 CH2 CH2 CH3 |
C、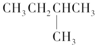 |
D、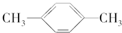 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com