
����Ŀ��ú������Ҫ�ĺ���������H2S�Լ�COS(�л���)��ú��ȼ�պ������ʻ�ת����SO2�Ӷ����������Ⱦ�����ú����H2S���ѳ��̶��ѳ�Ϊú���ྻ�ȵ�һ����Ҫָ�ꡣ��ش��������⣺
(1)�ѳ�ú����COS�ķ�����Br2��KOH��Һ��������H2��ԭ����ˮ�ⷨ�ȡ�
��COS�ķ��ӽṹ��CO2���ƣ�COS�ĽṹʽΪ___________��
��Br2��KOH��Һ��COS����Ϊ�����ε����ӷ���ʽΪ______________��
����֪��H2��COS��H2S��CO��ȼ��������Ϊ285kJ/mol��299kJ/mol��586kJ/mol��283kJ/mol��H2��ԭCOS�����ķ�ӦΪH2(g)+COS(g)=H2S(g)+CO(g)���÷�Ӧ����H=_________kJ/mol��
���º��������£��ܱ������н����尴n(H2)��n(COS)=2��1��Ϸ������з�Ӧ��������ʵ��˵����Ӧ�ﵽƽ��״̬����_______(����ĸ)
a.��������ƽ����Է����������ٸı� b. n(H2)��n(COS)�ı�ֵ����
c.CO������������� d.�γ�2 mol H-S����ͬʱ�γ�1 mol H-H��
���û�����-Al2O3��COSˮ�ⷴӦΪCOS(g)+H2O(g)![]() CO2(g)+H2S(g) ��H<0����ͬ�������ڴ�������ͣ����ͬʱ��ʱ����ͬ�¶���H2S��ת����(δ�ﵽƽ��)��ͼ��ʾ
CO2(g)+H2S(g) ��H<0����ͬ�������ڴ�������ͣ����ͬʱ��ʱ����ͬ�¶���H2S��ת����(δ�ﵽƽ��)��ͼ��ʾ

��ͼ��֪�������������ʱ��Ӧ���¶�ԼΪ______��H2S��ת�����ں����½���ԭ����_______________________________________��
(2)ú��ȼ�պ�������ת���ɵ�SO2�����Ա���ˮ���գ���֪25��ʱ��NH3��H2O��Kb=1.8��10-5��H2SO3��Ka1=1.3��10-2�� Ka2=6.2��10-8.��SO2ͨ�백ˮ�У�����Һ������ʱ����Һ�е�c(NH4+)/c(HSO3-)=_____________________.��ʱ��Һ�и�����Ũ�ȴ�С��ϵΪ��_____________________
���𰸡�O=C=SCOS+4Br2+12OH-=CO32-+SO42-+8Br-+6H2O285bcd150�� �����ж�����������Ӧ2.24 c(NH4+)> c(HSO3-)> c(SO32-)> c(H+)= c(OH-)
��������
��1����CO2�ĵȵ�����COS���ȵ�����ṹ���ƣ����ݶ�����̼�ķ��ӵĵ���ʽ��֪COS����ʽ����COS��Br2KOH��Ӧ����CO32-��SO42-��Br-��H2O���ݴ���д���ӷ���ʽ���۸��ݸ�˹�����жϢܵ��¶�Ϊ150��ʱ��COS��ת���������COS1mol��
��1����) COS��CO2�ĵȵ�����,�ȵ�����ṹ����,���ݶ�����̼�ķ��ӵĽṹʽ��֪COS�ṹʽ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��COS��Br2��KOH��Ӧ����K2CO3��K2SO4��KBr��H2O,�����ӷ���ʽΪCOS+4Br2+12OH�TCO32 + SO42 +8Br+6H2O���ʴ�Ϊ��COS+4Br2+12OH-=CO32-+SO42-+8Br-+6H2O ��
����֪��H2��COS��H2S��CO��ȼ��������Ϊ285kJ/mol��299kJ/mol ��586kJ/mol��283kJ/mol����ȼ���ȷ�Ӧ����ʽΪ����H2(g)+1/2O2(g)=H2O(l)��H=-285kJ/mol
��COS(g)+3/2O2(g)=CO2(g)+SO2(g) ��H=-299kJ/mol����H2S(g)+O2(g)=SO2(g)+H2O(l)��H=-586kJ/mol ��CO(g)+ 1/2O2(g)= CO2(g) ��H=-283kJ/mol������+��-��-��=-��285kJ/mol+299kJ/mol��+586kJ/mol+283kJ/mo=285 kJ/mol��H2��ԭCOS�����ķ�ӦΪH2(g)+COS(g)=H2S(g)+CO(g)���÷�Ӧ��H=+285kJ/mol��
a.��Ϊ������������ȵķ�Ӧ�����Ի�������ƽ����Է����������ٸı䲻����Ϊ�ж�ƽ������ݣ�b. ��Ϊ���尴n(H2)��n(COS)=2��1 Ͷ�ϣ�����n(H2)��n(COS)�ı�ֵ����ʱ˵���˷�Ӧ�ﵽƽ��״̬��c.CO�������������˵���˷�Ӧ�ﵽƽ��״̬ ��d.�γ�2 mol H-S����ͬʱ�γ�1 mol H-H��˵���˷�Ӧ�ﵽƽ��״̬ ���𰸣�bcd��
����ͼ��֪������ͬʱ���ڣ�ת�������ʱ�������Ļ������Ӧ���¶�Ϊ150�����¶ȹ��ߣ�ʹ�������Լ�����ɥʧ���������ж�������ת���ʼ�С������H2S��ת�����ں����½���ԭ���Ǵ����ж�����������Ӧ���𰸣�150�桢�����ж�����������Ӧ��
��2��NH3.H2O![]() NH4+ +OH-����Һ��c(NH4+)=c(OH-)��Kb=[ c(NH4+) c(OH-)]/ c(NH3.H2O) ��SO2ͨ�백ˮ�У���Һ�еĵ���غ�Ϊc(NH4+)+ c(H+)= c(HSO3-)+2 c(SO32-)+ c(OH-)������Һ������ʱc(OH-)= c(H+)����c(NH4+)= c(HSO3-)+2 c(SO32-)��K a2=[c(H+)
NH4+ +OH-����Һ��c(NH4+)=c(OH-)��Kb=[ c(NH4+) c(OH-)]/ c(NH3.H2O) ��SO2ͨ�백ˮ�У���Һ�еĵ���غ�Ϊc(NH4+)+ c(H+)= c(HSO3-)+2 c(SO32-)+ c(OH-)������Һ������ʱc(OH-)= c(H+)����c(NH4+)= c(HSO3-)+2 c(SO32-)��K a2=[c(H+)![]() c(SO32-)]/ c(HSO3-)��c(SO32-) Ka2/c(H+)��c(NH4+)=c(HSO3-)+2Ka2.c(HSO3-)/c(H+)=[1+2Ka2/c(H+)]c(HSO3-)��c(NH4+)/ c(HSO3-)=[1+2 Ka2/c(H+)=1+2
c(SO32-)]/ c(HSO3-)��c(SO32-) Ka2/c(H+)��c(NH4+)=c(HSO3-)+2Ka2.c(HSO3-)/c(H+)=[1+2Ka2/c(H+)]c(HSO3-)��c(NH4+)/ c(HSO3-)=[1+2 Ka2/c(H+)=1+2![]() 6.2��10-8
6.2��10-8![]() 1
1![]() 10-7=2.24.
10-7=2.24.
��ʱ��Һ�и�����Ũ�ȴ�С��ϵΪc(NH4+)> c(HSO3-)> c(SO32-)> c(H+)= c(OH-)���𰸣�2.24. c(NH4+)> c(HSO3-)> c(SO3



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£���aLNH3��ȫ����ˮ�õ�VmL��ˮ����Һ���ܶ�Ϊ![]() �����ʵ���������Ϊ�أ����ʵ����ʵ���Ũ��ΪC mol��L-1����������������ȷ����
�����ʵ���������Ϊ�أ����ʵ����ʵ���Ũ��ΪC mol��L-1����������������ȷ����
��![]() ��
��![]() ��������Һ���ټ���VmLˮ��������Һ��������������0.5��
��������Һ���ټ���VmLˮ��������Һ��������������0.5��
����������Һ�м���VmL C mol��L-1��ϡ���ᣬ��ַ�Ӧ����Һ������Ũ�ȴ�С��ϵΪ��![]()
A. �ڢ� B. �ڢ� C. �٢� D. �٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij����С��������CuO��NH3�ķ�Ӧ�о�NH3�������������ɣ����������ʵ��װ��(�г�װ��δ����)����ʵ�顣��ش��������⣺

��1������a������Ϊ________________������b�е��Լ�����Ϊ�����е�____________(����ĸ)
A�������� B����ʯ�� C��ʯ��ʯ D����ʯ��
��2��װ��B��������_______________
��3��ʵ���й۲쵽װ��C�к�ɫCuO��ĩ��Ϊ��ɫ���壬�������ռ�����ɫ��ζ�����壬д��װ��C�з�����Ӧ�Ļ�ѧ����ʽ_______________
��4��ʵ����ϣ�����ø����D����mg��װ��F�����������ΪnL(������ɱ�״��)�������е������ԭ�Ӹ�����Ϊ____________(�ú�m��n��ĸ�Ĵ���ʽ��ʾ)
���������������г��ý���
��1��д������ˮ�����ķ�Ӧ����ʽ______________________________��
��2���Ȼ�������Һ�ڿ������ױ�������������Һ�Ƿ���������Լ�Ϊ___________��д��ѧʽ�������Ȼ�������Һ�м����ռ���Һ������Ϊ_________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ���������Լ���ǩ�ϵIJ������ݣ��ݴ�����˵����ȷ���ǣ� ��

A. ����������ʵ���Ũ��Ϊ9.2mol/L
B. 1molAl�������ĸ����ᷴӦ����3g����
C. ����500mL4.6 mol/L��ϡ������ȡ������125mL
D. ���������ˮ�����������49%����Һʱ�����ʵ���Ũ�ȵ���9.2mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ�NaClO2����һ��ǿ������Ư�����㷺���ڷ�֯��ӡȾ��ʳƷ��ҵ����ҵ�������������ƺ�����Ĺ����������£�
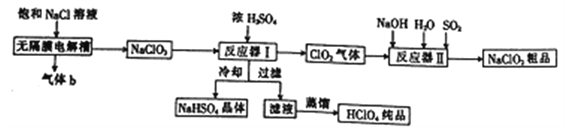
��֪��NaHSO4���ܽ�����¶ȵ����߶������ʵ������¿ɽᾧ��������ش��������⣺
(1)NaClO2����Ԫ�صĻ��ϼ�Ϊ_________��ij����NaCl��Һ�к���CaCl2��MgCl2��Na2SO4�����ʣ�ͨ�����¼���ʵ�鲽�裬���Ƶô�����ʳ��ˮ���������Թ�����Na2CO3��Һ���������Թ�����NaOH��Һ���������Թ�����BaCl2��Һ��������ϡ�����������ݲ����������ˡ���ȷ�IJ���˳����________��
(2)����b��______���ѧʽ������Ĥ�����������ĵ缫��ӦʽΪ___________��
(3)��Ӧ��I�з�����Ӧ�Ļ�ѧ����ʽΪ_________����ȴ��Ŀ����___________��
(4)��Ӧ��II�з�����Ӧ�����ӷ���ʽΪ________________��
(5)�����£�HClO2�ĵ���ƽ�ⳣ��Ka=1.07��10-2����Ӧ��II�з�Ӧ����NaClO2��Һ��������NaOH����pH=13������Һ��![]() =__________��
=__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������������������ȷ����
A. ͨ��״���£�1 mol SO3���еķ�����ΪNA
B. 1 mol OH�������⣬ת�Ƶĵ�����ĿΪNA
C. ��״���£���NA���ԭ�ӵ�������ԼΪ22.4 L
D. ��״���£�V Lˮ���е���ԭ����ԼΪVNA/22.4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2��һ��ɱ������Ч�ʸߡ�������ȾС��ˮ��������ʵ�����п�ͨ�����·�Ӧ�Ƶã�2KClO3��H2C2O4��H2SO4![]() 2ClO2����K2SO4��2CO2����2H2O������˵������ȷ������ ��
2ClO2����K2SO4��2CO2����2H2O������˵������ȷ������ ��
A��CO2����������
B��H2C2O4�ڷ�Ӧ�б�����
C��H2C2O4��������ǿ��ClO2��������
D��ClO2��ˮ������ʱ����������ǿ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�鷨��ѧϰ��ѧ����Ҫ������
�������к��зḻ�ĵ�Ԫ�أ��Ե����ӵ���ʽ���ڡ�ʵ������Ӻ�������ȡ�����������(��֪2I-��Cl2=2Cl-��I2��������һ���������л��ܼ�)��

��1��ʵ������ٵ����ƣ�___________________ ��
��2��ʵ�鲽����м�����Cl2��Ŀ����______________________________��
��3��ʵ�鲽�����ȡ��Ĺ����У�����ѡ�õ��ܼ���________��
A���� B���ƾ� C�����Ȼ�̼
��4���Ӻ��忪ʼ����5��������������л���Һ��ʵ���������Ҫ�õ�����ʵ����������֪ʵ������������������ǯ���ձ������������ƾ��ơ�ʯ�������Լ���Ҫ�ļг���������Ʒ����ȱ�ٵIJ���������__________________��________________��
��5���Ӻ�����л���Һ����ȡ��ͻ����л��ܼ������辭������ָ����ͼ��ʾʵ��װ���еĴ���֮����_________________��_________________��__________________��
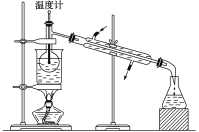
��ijѧ�����������ʵ�鷽������NaCl��CaCl2���ֹ�������:
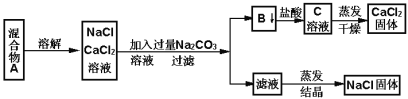
��պͻش���������
��1��д������B���ʵĻ�ѧ����ʽ________________
��2����Һ�е�������_____________________��д��ѧʽ������Ҫ�Ƶô�����NaCl��Ӧ����Һ�м���������ij���Լ������Լ���������_________________ ��
��3����Ҫ�ⶨ����Ʒ��NaCl��CaCl2�������ȣ��ɳ��������B���ʺ���һ���ʵ�����������������___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
A. NaNO2��Һ������KMnO4��Һ��2MnO4��+5NO2��+6H+�T2Mn2++5NO3��+3H2O
B. ̼�������Һ����������������Һ��NH4++HCO3��+2OH���TCO32��+NH3H2O+H2O
C. Fe��NO3��3��Һ�м��������HI��Һ��2Fe3++2I���T2Fe2++I2
D. �ö��Ե缫����Ȼ�����Һ��2Cl��+2H2O�TCl2��+H2��+2OH��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com