
| A.④>③=②>① | B.③=②<④<① | C.①>②>③>④ | D.④>③>②>① |
科目:高中化学 来源:不详 题型:单选题
| A.(Q1+Q2+Q3)kJ | B.0.5(Q1+Q2+Q3)kJ |
| C.(0.5Q1-1.5Q2+0.5Q3)kJ | D.((Q2-3Q1-Q3)kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.v(NH3)=0.2mol/(L?s) | B.v(N2)=1.0mol/(L?min) |
| C.v(H2)=1.67mol/(L?min) | D.v(H2)=0.3mol/(L?min) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等于0.6mol/L | B.小于0.6mol/L |
| C.等于0.8mol/L | D.大于0.8mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.v(O2) | B.v(NO) | C.v(H2O) | D.v(NH3) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
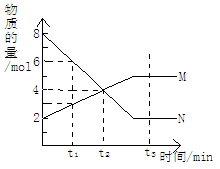
A.反应的化学方程式为:2M N N |
| B.t2时,正逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 |
| D.t1时,N的浓度是M浓度的2倍 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是
2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是| A.①④⑥⑦ | B.②③⑤⑦ |
| C.①③④⑤ | D.全部 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

 2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是( )
2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是( )| A.②④⑤⑥ | B.②③④⑤ | C.①③④⑤ | D.全部 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
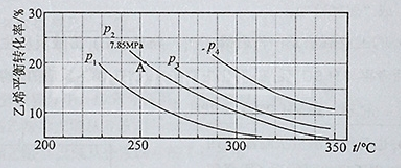
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com