
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是( )
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是( )
A.容器内压强不再改变B.v(H2O)=v(H2)
C.气体的密度不再改变D.反应不再进行
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】已知:用NH3催化还原NOx时包含以下反应.
反应①:4NH3 (g)+6NO(g) ![]() 5N2(g)+6H2O(l) H1=-1 807. 0 kJ·mol—1,
5N2(g)+6H2O(l) H1=-1 807. 0 kJ·mol—1,
反应②:4NH3(g)+6NO2(g) ![]() 5N2(g)+3O2(g)+6H2O(l) H2=?
5N2(g)+3O2(g)+6H2O(l) H2=?
反应③:2NO(g)+O2(g) ![]() 2NO2(g) H3=-113.0kJ·mol一1
2NO2(g) H3=-113.0kJ·mol一1
(1)反应②的H2==_____________。
(2)为探究温度及不同催化剂对反应①的影响.分别在不同温度、不同催化剂下.保持其他初始条件不变重复实验.在相同时间内测得N2浓度的变化情况如下图所示。

①反应①的平衡常数的表达式K=________。相同温度下.在催化剂甲的作用下反应的平衡常数______(填“大于”“小于”或“等于”)在催化剂乙的作用下反应的平衡常数。
②N点后N2浓度减小的原因可能是_____________________。
(3)某温度下,在1 L恒容密闭容器中初始投入4 mol NH3和6 mol NO发生反应①.当气体总物质的量为7.5mol时反应达到平衡.则NH3的转化率为____,达平衡所用时间为5 min.则用NO表示此反应0~5 min内的平均反应速率为______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或者结论正确的是( )
A.配制一定物质的量浓度的溶液时,容量瓶必须洁净、干燥,使用前还要检验是否漏水
B.实验室配制100.0 g,20%的氯化钠溶液,可取20.0 g的NaCl于烧杯中,再加入80.0 mL的水,充分搅拌后即可
C.实验室里需要480 mL 2.0 mol·L-1的氢氧化钠溶液,配制溶液时先称量氢氧化钠固体38.4 g,然后再按照溶解、冷却、移液、定容、摇匀等步骤进行操作
D.实验室配制500 mL 0.2 mol·L-1的硫酸亚铁溶液,如果在称量时把砝码和硫酸亚铁固体放反(其他操作都正确),则最终溶液浓度会偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是中学常见的五种化合物,它们之间有下列转化关系:
![]()
已知A溶液显碱性,焰色反应为黄色,且可促进水的电离。
(1)若A、B、C中含有相同的金属元素,且B为白色沉淀物,则A的化学式为____,D的化学式为_____;A、C反应生成B的离子方程式为___________。
(2)若C是一种无色无味的气体,用离子方程式表示A溶液显碱性的原因___________,C与E反应生成B的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式表示正确的是( )
A.向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO
B.AlCl3溶液中加入过量稀氨水:Al3++4NH3·H2O=AlO![]() +4NH
+4NH![]() +2H2O
+2H2O
C.稀HNO3与铁屑反应:Fe+2H+=Fe2++H2↑
D.FeCl2溶液中加入H2O2:2Fe2++H2O2+2H+=2Fe3++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
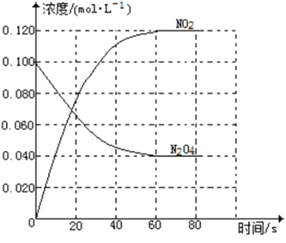
回答下列问题:
(1)反应的△H______0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为___________molL-1s-1反应的平衡常数K1为___________。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 molL-1s-1的平均速率降低,经10s又达到平衡。
①T_______100℃(填“大于”“小于”),判断理由是_____。
②列式计算温度T是反应的平衡常数K2___________
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向___________(填“正反应”或“逆反应”)方向移动,判断理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取和收集纯净干燥的氯气,并进行氯气性质探究的实验装置图:

(1)反应前,在__中装浓盐酸(填写仪器名称),__中装MnO2(填写仪器名称)。
(2)装置A中所装试剂是__,目的__。装置B中所装的试剂是___,目的__。
(3)装置D中所装试剂是__,发生反应的化学方程式为__。
(4)实验室制取Cl2的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某制碱制得的纯碱中含有NaHCO3和NaCl杂质。某实验小组对此碱样品进行检查。
(1)取此碱样品10g,加热到质量不再减少,冷却称重,称得质量为9.845g,该样品中NaHCO3的质量分数为__________________________。
(2)另取10g固体样品,加蒸馏水溶解,配成250mL一定物质的量浓度的溶液,配制过程中必需使用的化学仪器有______________________(填字母)
A.烧杯 B.250mL容量瓶C.漏斗 D.胶头滴管 E.玻璃棒 F.试管
(3)量取上述配制好的溶液25mL,向其中加入过量盐酸至 不再产生气泡,共收集到190.4mL(标准状况)气体,该反应过程的离子方程式为______________________、_______________________。10g该样品中含____________gNaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ka (HCOOH)=1.77×10-4,Ka (CH3COOH)=1.75×10-5,Kb (NH3·H2O) =1.76×10-5,下列说法正确的是( )
A. 将CH3COONa溶液从20℃升温至30℃,溶液中 增大
增大
B. 用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等
C. 0.2 mol/L HCOOH 与 0.1 mol/L NaOH 等体积混合后:c(HCOO-) + c(OH-) = c(HCOOH) + c(H+)
D. 0.2 mol/L CH3COONa 与 0.1 mol/L盐酸等体积混合后 (pH<7):c(CH3COO-) > c(Cl- ) >c(CH3COOH) >c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com