
【题目】氮的化合物在化工领域有重要的作用:
(1)以铁为催化剂,![]() mol氮气和
mol氮气和![]() mol氢气在恒温、容积恒定为1L的密闭容器中反应生成氨气,20min后达到平衡,氮气的物质的量为
mol氢气在恒温、容积恒定为1L的密闭容器中反应生成氨气,20min后达到平衡,氮气的物质的量为![]() mol。
mol。
①该条件下氮气的转化率是______,该温度下![]() 的化学平衡常数是______
的化学平衡常数是______![]() 保留小数点后两位
保留小数点后两位![]() 。
。
②在第25min时,保持温度不变,将容器体积迅速增大至2L并保持恒容,体系达到平衡时![]() 的总转化率为
的总转化率为![]() 氮气的转化率减小的原因是______。
氮气的转化率减小的原因是______。
③合成氨反应:![]()
![]() ,在反应过程中只改变一个条件,正反应速率的变化如图所示:
,在反应过程中只改变一个条件,正反应速率的变化如图所示:![]() 时改变的条件是______;
时改变的条件是______;![]() 时改变的条件是______。
时改变的条件是______。

(2)①![]() 是一种高能燃料,有强还原性,可通过
是一种高能燃料,有强还原性,可通过![]() 和NaClO反应制得,写出该制备反应的化学方程式______。
和NaClO反应制得,写出该制备反应的化学方程式______。
②N2H4的水溶液呈弱碱性,室温下其电离常数![]() ,则
,则![]()
![]() 水溶液的pH等于______
水溶液的pH等于______![]() 忽略
忽略![]() 的二级电离和
的二级电离和![]() 的电离
的电离![]() 。
。
③已知298K和101kPa条件下:
![]()
![]()
![]()
![]()
则![]() 的燃烧热
的燃烧热![]() ______。
______。
【答案】![]()
![]() 扩大体积,压强减小,化学平衡逆向移动,氮气的转化率减小 加入催化剂 减小生成物浓度
扩大体积,压强减小,化学平衡逆向移动,氮气的转化率减小 加入催化剂 减小生成物浓度 ![]() 10
10 ![]()
【解析】
![]() 氮气转化率
氮气转化率 ;化学平衡常数
;化学平衡常数 的公式进行解答;
的公式进行解答;![]() 扩大体积,相当于减小压强,平衡向气体体积增大的方向移动;
扩大体积,相当于减小压强,平衡向气体体积增大的方向移动;![]() 时改变条件时平衡不移动,改变条件时能同等程度的增大正逆反应速率;
时改变条件时平衡不移动,改变条件时能同等程度的增大正逆反应速率;![]() 时改变条件时,达到平衡状态反应速率降低,则逆反应速率减小,为减小生成物浓度;
时改变条件时,达到平衡状态反应速率降低,则逆反应速率减小,为减小生成物浓度;
![]() 可通过
可通过![]() 和NaClO反应制得,该反应中N元素化合价由
和NaClO反应制得,该反应中N元素化合价由![]() 价变为
价变为![]() 价、Cl元素化合价由
价、Cl元素化合价由![]() 价变为
价变为![]() 价,生成氯化钠,同时生成水;
价,生成氯化钠,同时生成水;
![]() 该溶液中溶质电离程度较小,则
该溶液中溶质电离程度较小,则![]() ,该溶液中
,该溶液中![]() ,溶液中
,溶液中![]() 。
。
![]() 内消耗的
内消耗的![]() ,氮气转化率
,氮气转化率 ;开始时
;开始时![]() 、
、![]() ,消耗
,消耗![]() ,
,

化学平衡常数 ,故答案为:
,故答案为:![]() ;
;![]() ;
;
![]() 扩大体积,相当于减小压强,平衡向气体体积增大的方向移动向逆反应方向移动,则氮气转化率降低,故答案:扩大体积,压强减小,化学平衡逆向移动,氮气的转化率减小;
扩大体积,相当于减小压强,平衡向气体体积增大的方向移动向逆反应方向移动,则氮气转化率降低,故答案:扩大体积,压强减小,化学平衡逆向移动,氮气的转化率减小;
![]() 时改变条件时平衡不移动,改变条件时能同等程度的增大正逆反应速率,平衡不移动,且该反应前后气体体积改变,所以改变的条件是加入催化剂;
时改变条件时平衡不移动,改变条件时能同等程度的增大正逆反应速率,平衡不移动,且该反应前后气体体积改变,所以改变的条件是加入催化剂;![]() 时改变条件时,达到平衡状态反应速率降低,则逆反应速率减小,为减小生成物浓度,故答案:加入催化剂;减小生成物浓度;
时改变条件时,达到平衡状态反应速率降低,则逆反应速率减小,为减小生成物浓度,故答案:加入催化剂;减小生成物浓度;
![]() 可通过
可通过![]() 和NaClO反应制得,该反应中N元素化合价由
和NaClO反应制得,该反应中N元素化合价由![]() 价变为
价变为![]() 价、Cl元素化合价由
价、Cl元素化合价由![]() 价变为
价变为![]() 价,生成氯化钠,同时生成水,反应方程式为
价,生成氯化钠,同时生成水,反应方程式为![]() ,故答案:
,故答案:![]() ;
;
![]() 该溶液中溶质电离程度较小,则
该溶液中溶质电离程度较小,则![]() ,该溶液中
,该溶液中![]() ,溶液中
,溶液中![]() ,则溶液的
,则溶液的![]() ,故答案为:10;
,故答案为:10;
![]() ,
,![]() ,
,![]() ,
,![]()
将方程式![]() 得
得![]() ,则
,则![]() ,
,
故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】![]() 时,下列溶液中微粒的物质的量浓度关系正确的是
时,下列溶液中微粒的物质的量浓度关系正确的是
A.![]() 的盐酸与
的盐酸与![]() 的
的![]() 溶液混合后:
溶液混合后:![]()
B.![]() 的NaHS溶液中:
的NaHS溶液中:![]()
![]()
C.100mL![]() 的
的![]()
![]() 溶液和10mL
溶液和10mL![]() 的
的![]() 溶液混合后
溶液混合后![]() 忽略混合后溶液体积变化
忽略混合后溶液体积变化![]() :
:![]()
D.![]() 的HCN溶液和
的HCN溶液和![]() 的NaCN溶液等体积混合后
的NaCN溶液等体积混合后![]() :
:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是( )
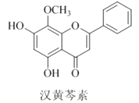
A.汉黄芩素的分子式为C16H13O5
B.该物质中含有四种含氧官能团
C.1mol该物质与溴水反应,最多消耗2molBr2
D.与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是![]()
a.锌跟足量稀硫酸反应时,加入少量硫酸铜溶液能加快反应速率且不影响产气量
b.镀层破损后,白铁![]() 镀锌的铁
镀锌的铁![]() 比马口铁
比马口铁![]() 镀锡的铁
镀锡的铁![]() 更易腐蚀
更易腐蚀
c.电镀时,应把镀件置于电解槽的阴极
d.冶炼铝时,可以电解熔融态的![]()
e.钢铁表面常易锈蚀生成![]()
A.abcdeB.acdeC.ceD.bd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行X2(g)+3Y2(g)![]() 2Z(g)的反应,其X2、Y2、Z的起始浓度依次为0.1 mol/L、0.3 mol/L、0.2 mol/L,当反应达平衡时,各物质的浓度有可能的是 ( )
2Z(g)的反应,其X2、Y2、Z的起始浓度依次为0.1 mol/L、0.3 mol/L、0.2 mol/L,当反应达平衡时,各物质的浓度有可能的是 ( )
A.c(Z)=0.5 mol/LB.c(Z)=0.4 mol/L
C.c(X2)=0.2 mol/L或c(Y2)=0.6 mol/LD.c(Y2)=0.5 mol/L或c(X2)=0.15 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用标准NaOH溶液来测定未知浓度的盐酸的浓度:
(1)先配制250mL 0.5mol/L的NaOH标准溶液所需的称量的质量NaOH为________ g,
需要的主要玻璃仪器有玻璃棒、量烧杯、胶头滴管、量筒和___________。
(2)用滴定管准确量取20.00mL未知浓度的盐酸于锥形瓶中,加入酚酞作指示剂,用NaOH溶液滴定到终点。在锥形瓶的待测液中滴加2~3滴酚酞试液,并开始滴定。
手眼:左手控制滴定管活塞,右手摇动锥形瓶,眼睛____________;
滴速:先快后慢,当接近终点时,应一滴一摇。滴定终点的判断:___________,即到终点,读出体积并记录数据。
(3)该同学进行了三次实验,实验数据如下表:
实验编号 | 盐酸的体积(mL) | 标准NaOH溶液的体积(mL) |
① | 均是20.00 | 16.90 |
② | 17.10 | |
③ | 18.20 |
滴定中误差较大的是第______次实验。造成这种误差的可能原因是__________(填选项编号)
a.滴定管在盛装标准NaOH溶液前未润洗
b.在盛装未知浓度的盐酸之前锥形瓶里面有少量蒸馏水,未烘干
c.达到滴定终点时,俯视溶液凹液面最低点读数
d.滴定开始前盛装标准NaOH溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
e.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
f.滴定开始前盛装标准NaOH溶液的滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡
(4)该同学所测得盐酸的物质的量浓度为_________。(结果保留三位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g) ![]() 2C(g)+2D(g)在四种不同情况下的反应速率分别为①v(A)=0.15 mol·L-1·s-1 ②v(B)=0.6 mol·L-1·s-1;③v(C)=0.4 mol·L-1·s-1;④v(D)=0.45 mol·L-1·s-1该反应进行的快慢顺序为( )
2C(g)+2D(g)在四种不同情况下的反应速率分别为①v(A)=0.15 mol·L-1·s-1 ②v(B)=0.6 mol·L-1·s-1;③v(C)=0.4 mol·L-1·s-1;④v(D)=0.45 mol·L-1·s-1该反应进行的快慢顺序为( )
A.④>②=③>①B.④>②>③>①
C.①>②=③>④D.①>②>③>④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从下列事实所得出的解释或结论正确的是
选项 | 实验事实 | 解释或结论 |
A | 已知 | 金刚石比石墨稳定 |
B |
| 这是一个熵增反应 |
C | 已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动 | 反应物的转化率一定增大 |
D | 用醋酸作导电性实验时,灯泡很暗 | 说明醋酸是弱酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
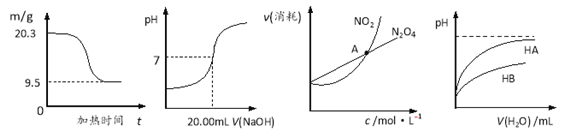
图1 图2 图3 图4
A. 图1表示0.1molMgCl2·6H2O在空气中充分加热时固体质量随时间的变化
B. 图2表示用0.1000 mol·LˉlNaOH溶液滴定25.00 mLCH3COOH的滴定曲线,则c(CH3COOH)=0.0800 mol·Lˉ1
C. 图3表示恒温恒容条件下,2NO2(g)![]() N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
D. 图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则常温下,NaA溶液的pH小于同浓度的NaB溶液的pH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com