
用石墨做电极电解CuSO4溶液.通电一段时间后,欲使用电解液恢复到起始状态,应向溶液中加入适量的( )
|
| A. | CuSO4 | B. | H2O | C. | CuO | D. | CuSO4•5H2O |
考点:
电解原理.
专题:
电化学专题.
分析:
用铂电极电解CuSO4溶液,阴极铜离子放电,阳极氢氧根离子放电,然后根据析出的物质向溶液中加入它们形成的化合物即可;
解答:
解:CuSO4溶液存在的阴离子为:SO42﹣、OH﹣,OH﹣离子的放电能力大于SO42﹣ 离子的放电能力,所以OH﹣离子放电生成氧气;
溶液中存在的阳离子是Cu2+、H+,Cu2+离子的放电能力大于H+离子的放电能力,所以Cu2+离子放电生成Cu;
溶液变成硫酸溶液;
电解硫酸铜的方程式为:2CuSO4+2H2O 2 Cu+O2 ↑+2H2SO4,
2 Cu+O2 ↑+2H2SO4,
所以从溶液中析出的物质是氧气和铜,因为氧气和铜和稀硫酸都不反应,但和氧化铜反应,氧气和铜反应生成氧化铜,所以向溶液中加入氧化铜即可,
故选C.
点评:
本题考查了电解原理,能正确判断溶液中离子的放电顺序从而确定析出的物质是解本题的关键,难度不大.


 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
已知镁和稀硝酸反应时,每有1 molHNO3 反应,就有0.8mol电子转移,此时硝酸的还原产物可能是 ( )
A.NO2 B.N2O C.N2O3 D.NO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中,溶质的物质的量浓度为1 mol•L-1的是( )
A.将40 g NaOH溶于1 L水中所得的溶液
B.将22.4 L HCl溶于水配成1 L溶液
C.含K+的物质的量为2 mol的K2SO4溶液1 L
D.将0.5 mol•L-1的NaNO3溶液100 mL加热蒸发掉50 g水的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
铬是人体必需的微量元素,但铬过量会引起污染,危害人体健康。不同价态的铬毒性不一样,六价铬的毒性最大。下列叙述错误的是( )
A.K2Cr2O7可以氧化乙醇,可用来鉴别司机是否酒后驾驶
B.污水中铬一般以Cr3+存在,与水中的溶解氧作用可被还原为六价铬
C.人体内六价铬超标,服用维生素C缓解毒性,说明维生素C具有还原性
D.1 mol 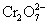 得到6 mol电子时,还原产物是Cr3+
得到6 mol电子时,还原产物是Cr3+
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.Na2O2+2HCl====2NaCl+H2O2
B.Ag2O+H2O2====2Ag+O2↑+H2O
C.2H2O2====2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH====2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2仅体现氧化性的反应是(填序号,下同) ,H2O2既体现氧化性又体现还原性的反应是 。
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序是 。
(3)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:
O2、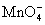 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。
①反应体系选择的酸是: (填序号)。
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸
②如果上述反应中有6.72 L(标准状况)气体生成,转移的电子为 mol。
(4)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应:KCN+H2O2+H2O====A+NH3↑,试指出生成物A的化学式为 ,并阐明H2O2被称为绿色氧化剂的理由是
。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于化学平衡常数的叙述中,正确的是( )
|
| A. | 只与化学反应本身和温度有关 |
|
| B. | 只与反应的温度有关 |
|
| C. | 与化学反应本身和温度有关,并且会受到起始浓度的影响 |
|
| D. | 只与化学反应本身有关,与其他任何条件无关的一个不变的常数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
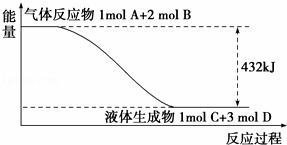
某反应过程中的能量变化如图所示:
(1)写出该反应的热化学方程式:
(2)在溶液中进行化学反应中的物质,其状态标为“aq”,已知0.5mol H2SO4在溶液中与足量氢氧化钠反应放出57.3kJ的热量,用离子方程式写出该反应的热化学方程式: .
(3)合成氨反应的热化学方程式:
N2(g)+3H2(g)⇌2NH3(g)△H=﹣92.2kJ•mol﹣1
已知合成氨反应是一个反应物不能完全转化为生成物的反应,在某一定条件下,N2的转化率仅为10%,要想通过该反应得到92.2kJ的热量,至少在反应混合物中要投放N2的物质的量为 mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
从下列实验事实所得出的结论,正确的是()
实验事实 结论
① Cl2的水溶液可以导电 Cl2是电解质
② 常温下,0.1mol•L﹣1NaA与NaB溶液的pH前者大 酸性:HA<HB
③ 常温下,白磷可自燃而硫不与氧气反应 非金属性:P>S
④ 某溶液中滴加KSCN溶液,溶液变为血红色 该溶液含有Fe3+
A. ③④ B. ②④ C. ①② D. 全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com