
分析 发生Fe+2HCl=FeCl2+H2↑,该反应生成了2.24L H2(标准状况下),气体的物质的量为$\frac{2.24L}{22.4L/mol}$=0.1mol,结合反应及V=$\frac{n}{c}$、元素的化合价变化计算.
解答 解:(1)气体的物质的量为$\frac{2.24L}{22.4L/mol}$=0.1mol,由Fe+2HCl=FeCl2+H2↑可知消耗Fe的物质的量为0.1 mol,
答:消耗Fe的物质的量为0.1mol;
(2)由反应可知消耗HCl为0.1mol×2=0.2mol,则需要盐酸的体积为$\frac{0.2mol}{2mol/L}$=0.1 L,
答:至少需该盐酸为0.1L;
(3)生成氢气为0.1mol,则生成的H2所转移的电子数是0.1mol×2×(1-0)×NA=0.2NA或1.204×1023,
答:生成的H2所转移的电子数是0.2NA或1.204×1023个.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应、转移电子的计算为解答的关键,侧重分析与计算能力的考查,注意物质的量的相关计算,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
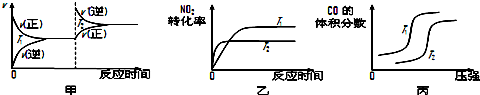
| 起始物质的量 | 甲 | 乙 | 丙 |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(O2)>m(CO2) | |
| B. | 当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(02)>ρ(C02) | |
| C. | 当它们的质量和温度、压强均相同时,三种气体的体积:V(CO2)>V(O2)>V(H2) | |
| D. | 当它们的温度和密度都相同时,三种气体的压强:P(H2)>P(O2)>P(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要称量NaClO固体的质量为144.0 g | |
| B. | 如图所示的仪器中,有四种是不需要的,另外还需一种玻璃仪器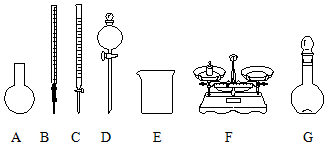 | |
| C. | 配制的溶液在空气中光照,久置后溶液中NaClO的物质的量浓度减小 | |
| D. | 容量瓶用蒸馏水洗净后应烘干才能用于溶液配制,否则结果偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +172.22kJ/mol | B. | -172.22kJ/mol | C. | -392.92kJ/mol | D. | +392.92kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在城区内汽车限行,限制燃煤锅炉的使用 | |
| B. | 容易产生扬尘的工厂和建筑工地停工 | |
| C. | 在灰尘较多的道路洒水,以减少扬尘的产生 | |
| D. | 要求市民出行时一定要戴防雾霾专用口罩 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com