
| A. | 4mol | B. | 8mol | C. | 16mol | D. | 24mol |
科目:高中化学 来源: 题型:多选题
| A. | 10.7g | B. | 21.4g | C. | 23.9g | D. | 40g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3能与NaOH溶液反应,则Al(OH)3也能与氨水反应 | |
| B. | Al、Al2O3、Al(OH)3都可溶于NaOH溶液和盐酸中 | |
| C. | 向AlCl3溶液中滴加氨水,产生白色沉淀,再加过量NaHSO4溶液,沉淀消失 | |
| D. | 能用同一个离子方程式表示:氨水滴入Al2(SO4)3溶液和Al2(SO4)3溶液滴入浓氨水的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 缩小体积使压强增大 | B. | 体积不变充入N2使压强增大 | ||
| C. | 体积不变充入He使气体压强增大 | D. | 总压强不变充入Ne |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 31g•mol-1 | B. | 32g•mol-1 | C. | 33g•mol-1 | D. | 17g•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ③④ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
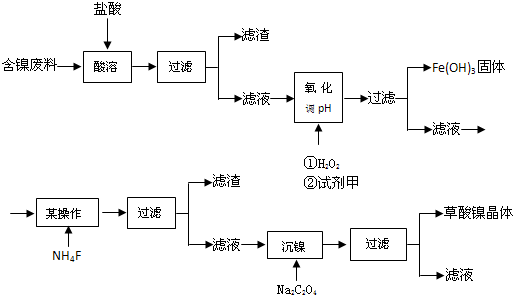
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com