
【题目】将一定量的SO2(g)和O2(g)分别通入体积为2L的恒容密闭容器中,在不同温度下进行反应:
2 SO2(g)+ O2(g)![]() 2SO3△H<0。得到如表中的两组数据:
2SO3△H<0。得到如表中的两组数据:
实验编号 | 温度/℃ | 平衡常数/mol-1·L | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | ||||
1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
下列说法不正确的是
A.x= 1.6,y=0.2 ,t<6
B.T1、T2的关系:T1 > T2
C.K1、K2的关系:K2>K1
D.实验1在前6min的反应速率υ(SO2)=0.2 mol·L-1·min-1
【答案】A
【解析】
试题分析:A、实验1从开始到反应达到化学平衡时,
2SO2(g)+O2(g) ![]() 2SO3(g)
2SO3(g)
起始量(mol) 4 2 0
变化量(mol) 2.4 1.2 2.4
平衡量(mol) x 0.8 2.4
x=4-2.4=1.6;
实验2从开始到反应达到化学平衡时,
2SO2(g)+O2(g)![]() 2SO3(g)
2SO3(g)
起始量(mol) 4 2 0
变化量(mol) 3.6 1.8 3.6
平衡量(mol) 0.4 y 3.6
y=2-1.8=0.2;
该反应为放热反应,升高温度平衡逆向移动,二氧化硫的物质的量增加,所以温度是T1>T2。温度高反应速率快,到达平衡的时间少,则t>6,A错误;B、根据A中分析可知B正确;C、由于T1>T2,所以K2>K1,C正确;D、实验1在前6 min的反应速率v (SO2)=![]() =0.2 mol·L-1·min-1,D正确,答案选A。
=0.2 mol·L-1·min-1,D正确,答案选A。


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】下面提到的情况中,与盐的水解有关的是
①明矾和FeCl3可作净水剂②为保存FeCl3溶液,要在溶液中加少量盐酸③实验室配制AlCl3溶液时,应先把它溶解在盐酸中,而后加水稀释④NH4Cl溶液可作焊接中的除锈剂⑤实验室盛放Na2SiO3溶液的试剂瓶应用橡皮塞,而不能用玻璃塞⑥用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂⑦在NH4Cl或AlCl3溶液中加入金属镁会生成氢气⑧草木灰与铵态氮肥不能混合施用⑨加热蒸干AlCl3溶液得到Al(OH)3固体
A.①④⑦ B.②⑤⑧ C.③⑥⑨ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将m体积NO2和n体积O2同时通入倒立于水中且盛满水的容器内,充分反应后,容器内残留![]() 体积的气体,该气体与空气接触未变为红棕色,则m与n的比值为
体积的气体,该气体与空气接触未变为红棕色,则m与n的比值为
A. 3∶4 B. 4 ∶3 C. 8∶3 D. 3∶8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于能层和能级的说法正确的是
A. 3p2表示3p能级有两个轨道
B. 能层序数越大的能级能量不一定越高
C. 同一原子中,1s、2s、3s电子的能量逐渐减小
D. 同一原子中,2p、3p、4p能级的轨道数依次增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
①钠、氢气都能在氯气中燃烧生成白色烟雾
②铜丝在氯气中燃烧,生成蓝绿色的氯化铜
③液氯就是氯气的水溶液,它能使干燥的有色布条褪色
④久置的氯水,因氯气几乎完全挥发掉,剩下的就是水
A.只有① B.①和② C.①和④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列转化关系(反应条件略):
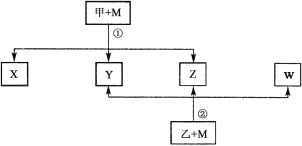
已知:① X 、Y 、Z 、W 均为氧化物。常态下,X 是红棕色气体;Y 能使澄清石灰水变浑浊但不能使品红溶液褪色。② 相对分子质量:甲﹤乙 。③ 将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的浓溶液露置在空气中一段时间,质量增加浓度降低。请填写下列空白:
(1)Z的化学式: 。
(2)将乙的浓溶液露置在空气中一段时间,质量增加浓度降低,反映出乙的浓溶液具有 性。利用这种性质可以进行 项(填字母)实验操作。
a.钝化铁片 b.检验Ba2+离子 c.干燥氨气 d.干燥氯气
(3)在 X 和 Z 的反应中,被氧化的X 与被还原的X 的物质的量之比是: 。
(4)W可用于工业制溴过程中吸收潮湿空气中的Br2 ,写出该反应的离子方程式: 。
(5)写出M与甲的浓溶液在加热条件下反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明代著名哲学家、科学家方以智在其《物理小识》卷七《金石类》中指出:有硇水者,剪银塊投之,则旋而为水。其中的“硇水”指
A. 醋酸 B. 盐酸 C. 硝酸 D. 硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用硫铁矿石(主要成分FeS2)在沸腾炉中焙烧,经过一系列反应,得到硫酸,焙烧后的矿渣用于炼铁。其转化过程如下图所示(部分条件、反应物和产物已略去):

请回答下列问题:
(1)在上面转化过程中,硫元素被氧化的反应是________(填反应编号)。
(2)写出反应②中炼铁的化学方程式_____________。若用1000t含杂质28%的矿渣炼铁,理论上可得到含铁96%的生铁质量为_____________ t.
(3)写出反应①的化学方程式 ,若有12.0g FeS2参加反应,则发生转移的电子数为 。
(4)烟气中SO2的排放会造成酸雨,工业上常用Na2SO3溶液来吸收SO2以减少对环境的危害。
①常温下,将SO2通入一定体积的1.0mol·L-1Na2SO3溶液中,溶液pH不断减小。当溶液pH约为6时,吸收SO2的能力显著下降,此时溶液中c(SO32-)的浓度是0.2mol·L-1,则溶液中c(HSO3-)是 mol·L-1。用化学平衡原理解释此时溶液显酸性的原因 。
②向①中pH约为6时的吸收液中通入足量O2充分反应。取反应后溶液10mL与10mLBaCl2溶液混合,欲使混合时能生成沉淀,所用BaCl2溶液的浓度不得低于 mol·L-1。[已知25℃时,Ksp(BaSO3)=5.48×10-7, Ksp(BaSO4)= 1.08×10-10]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式可用H++OH-═H2O表示的是
A. 醋酸与KOH溶液反应
B. 稀硫酸与Ba(OH)2溶液反应
C. NaHSO4溶液与NaOH溶液反应
D. 盐酸与氨水反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com