
| H2O2 |
 ,B发生加聚反应生成E为
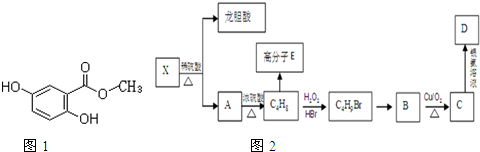
,B发生加聚反应生成E为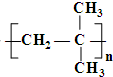 ,B与HBr在过氧化氢条件下发生加成反应,H原子加在含氢较少的碳原子上,反应生成(CH3)2CHCH2Br,B能类型发生氧化反应,则(CH3)2CHCH2Br再氢氧化钠水溶液、加热条件下发生水解反应生成B为(CH3)2CHCH2OH,则C为(CH3)2CHCHO,D为(CH3)2CHCOOH,据此解答.
,B与HBr在过氧化氢条件下发生加成反应,H原子加在含氢较少的碳原子上,反应生成(CH3)2CHCH2Br,B能类型发生氧化反应,则(CH3)2CHCH2Br再氢氧化钠水溶液、加热条件下发生水解反应生成B为(CH3)2CHCH2OH,则C为(CH3)2CHCHO,D为(CH3)2CHCOOH,据此解答.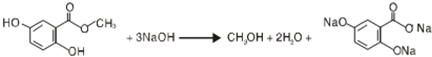 ,
, ;
; ,B发生加聚反应生成E为
,B发生加聚反应生成E为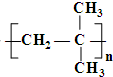 ,B与HBr在过氧化氢条件下发生加成反应,H原子加在含氢较少的碳原子上,反应生成(CH3)2CHCH2Br,B能类型发生氧化反应,则(CH3)2CHCH2Br再氢氧化钠水溶液、加热条件下发生水解反应生成B为(CH3)2CHCH2OH,则C为(CH3)2CHCHO,D为(CH3)2CHCOOH,
,B与HBr在过氧化氢条件下发生加成反应,H原子加在含氢较少的碳原子上,反应生成(CH3)2CHCH2Br,B能类型发生氧化反应,则(CH3)2CHCH2Br再氢氧化钠水溶液、加热条件下发生水解反应生成B为(CH3)2CHCH2OH,则C为(CH3)2CHCHO,D为(CH3)2CHCOOH, ,
, ;
;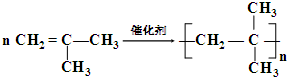 ,
,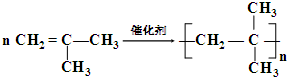 ;
;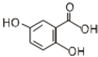 ,它的同分异构体满足下列条件:能使FeCl3溶液显色,含有酚羟基;属于酯类且能发生银镜反应,还含有-OOCH,含有2个酚羟基(-OH)、1个-OOCH时,2个酚羟基处于邻位,-OOCH有2种位置,2个酚羟基处于间位,-OOCH有3种位置,2个酚羟基处于对位,-OOCH有1种位置,故符合条件的同分异构体有2+3+1=6种,故答案为:6;
,它的同分异构体满足下列条件:能使FeCl3溶液显色,含有酚羟基;属于酯类且能发生银镜反应,还含有-OOCH,含有2个酚羟基(-OH)、1个-OOCH时,2个酚羟基处于邻位,-OOCH有2种位置,2个酚羟基处于间位,-OOCH有3种位置,2个酚羟基处于对位,-OOCH有1种位置,故符合条件的同分异构体有2+3+1=6种,故答案为:6;| Cu |
| △ |
| Cu |
| △ |


科目:高中化学 来源: 题型:
| A、标准状况下,4.48L水中含有的分子数目为0.2NA |
| B、0.1mol钠与足量水反应转移的电子数目为0.1NA |
| C、0.2mol?L-1CuSO4溶液中含有的SO42-离子数目为0.2NA |
| D、0.5molKClO3中含有Cl-的数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

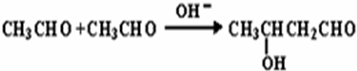
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定序号 | 待测液体积 | 所消耗盐酸标准的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 25.00 | 0.50 | 20.60 |
| 2 | 25.00 | 6.00 | 26.00 |
| 3 | 25.00 | 1.10 | 21.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
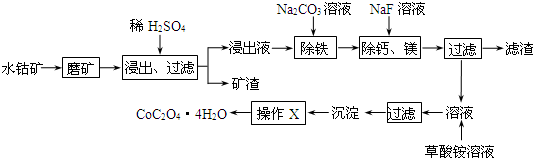
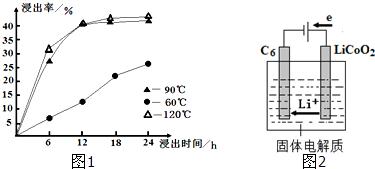
| c(Ca2+) |
| c(Mg2+) |
| 充电 |
| 放电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com