
| A.Fe与Al 的物质的量之比为1:1 |
| B.混合气体中NO为0.03mol ,N2O为0.12mol |
| C.原HNO3溶液的浓度C=4.9mol/L |
| D.反应中被还原的HNO3为0.15mol |


科目:高中化学 来源:不详 题型:填空题
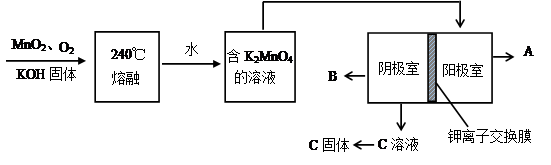
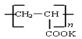 ),聚丙烯酸钾单体的结构简式为 。
),聚丙烯酸钾单体的结构简式为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应后溶液中c(NO3-)=0.85 mol·L-1 |
| B.反应后的溶液最多还能溶解1.82 g Fe |
| C.反应前HNO3溶液的浓度为1.0 mol·L-1 |
| D.1.12 L气体是NO、NO2的混合气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.爆竹爆炸不宜使用水来灭火,可用干沙 |
| B.爆竹的燃放产生大量污染气体,应加以限制 |
| C.爆竹燃放过程中硝酸钾作氧化剂 |
D.爆竹爆炸过程中发生反应为2KNO3+3C+S K2S+N2↑+3CO2↑,每生成1 mol N2转移10NA个电子(NA表示阿伏加德罗常数的值) K2S+N2↑+3CO2↑,每生成1 mol N2转移10NA个电子(NA表示阿伏加德罗常数的值) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.维生素C具有还原性 |
| B.上述过程中砷元素发生还原反应 |
| C.上述过程中+5价砷类物质作氧化剂 |
| D.1 mol+5价砷完全转化为+3价砷,共失去2 mol电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②=③>① | B.①>②=③ | C.②>③>① | D.①=②>③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2O2是氧化剂,H2O2中的氧元素被还原 |
| B.每生成1 mol O2转移的电子的物质的量为4 mol |
| C.ClO2中的氯元素被氧化 |
| D.ClO2是氧化剂,H2O2是还原剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原废液中含有的金属阳离子只有Fe2+和Cu2+ |
| B.该工厂原来使用的FeCl3溶液的物质的量浓度约为2 mol/L |
| C.若向500 mL废液中加入足量的稀HNO3溶液,在标况下产生NO气体4.48 L,则原废液中Fe2+和Cu2+的物质的量浓度之比为2:1 |
| D.可以使用硫氰化钾溶液检验该废液中是否含有Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com