
| A、还原性:Sn2+>Fe2+>Ce3+ |
| B、还原性:Fe2+>Ce3>+Sn2+ |
| C、氧化性:Sn4+>Ce4>+Fe3+ |
| D、氧化性:Ce4>+Fe3+>Sn4+ |
科目:高中化学 来源: 题型:
| A、提取碘水中的碘单质时,应选择有机萃取剂,且萃取剂与水不互溶 |
| B、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、蒸馏操作时,冷凝水方向应当由下往上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Na2O2+2H2O=4NaOH+O2 |
| B、CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 |
| C、SO3+H2O=H2SO4 |
| D、Na2O+H2O=2NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
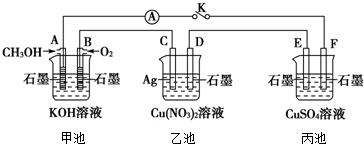
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生成物总能量一定低于反应物总能量 |
| B、应用盖斯定律,可计算某些难以直接测量的反应的焓变 |
| C、放热反应的反应速率总是大于吸热反应的反应速率 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H1>△H2>△H3 |
| B、△H1<△H3<△H2 |
| C、△H1<△H2<△H3 |
| D、△H1>△H3>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com