
| A. | 气态氢化物的稳定性按X、Y、Z的顺序递增 | |
| B. | 三种元素的最高价氧化物对应的水化物酸性:H2ZO3>H3YO4>H2XO4 | |
| C. | 元素的最高正化合价按X、Y、Z的顺序递增 | |
| D. | 元素原子的半径按X、Y、Z的顺序递增 |
分析 同周期的X、Y、Z三种元素,它们的气态氢化物的化学式为H2X、YH3、ZH4,X、Y、Z最低负化合价分别为-2、-3、-4,原子序数依次减小,同主族自左而右非金属性增强,氢化物稳定性减弱、最高价含氧酸的酸性增强、最高正化合价增大、原子半径减小.
解答 解:同周期的X、Y、Z三种元素,它们的气态氢化物的化学式为H2X、YH3、ZH4,X、Y、Z最低负化合价分别为-2、-3、-4,原子序数依次减小.
A.同周期X、Y、Z的原子序数依次减小,非金属性减弱,氢化物稳定性减弱,故A错误;
B.同周期X、Y、Z的原子序数依次减小,非金属性减弱,最高价含氧酸的酸性依次减弱,即酸性H4ZO4<H3YO4<H2XO4,故B错误;
C.同周期X、Y、Z的原子序数依次减小,最外层电子数依次减小,最高正化合价依次减小,故C错误;
D.同周期X、Y、Z的原子序数依次减小,原子半径增大,故D正确,
故选D.
点评 本题考查元素周期律,难度不大,注意对元素周期律的理解掌握,有利于基础知识的巩固.


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
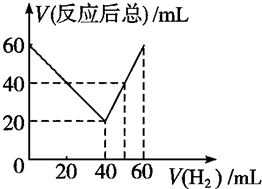 某气态不饱和链烃CnHm在一定条件下与H2加成为CnHm+x,取CnHm和H2混合气体共60mL进行实验,发现随混合气中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温同压下测定).由此可知x的数值为( )
某气态不饱和链烃CnHm在一定条件下与H2加成为CnHm+x,取CnHm和H2混合气体共60mL进行实验,发现随混合气中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温同压下测定).由此可知x的数值为( )| A. | 4 | B. | 3 | C. | 2 | D. | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时负极反应为:Zn-2e-+2OH--Zn(OH)2 | |
| B. | 放电时正极发生氧化反应 | |
| C. | 放电时每转移2mol电子,反应的锌的质量是65g | |
| D. | 放电时化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径是第ⅡA族中最大的 | B. | 遇冷水能剧烈反应 | ||
| C. | 位于第七周期 | D. | Ra(OH)2是两性氢氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ | |
| B. | HS-水解的离子方程式:HS-+H2O?S2-+H3O+ | |
| C. | CO32-水解的离子方程式:CO32-+2 H2O?H2CO3+2OH- | |
| D. | 用FeS为沉淀剂除去废水中的Hg2+:FeS(s)+Hg2+(aq)=HgS(s)+Fe2+(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数是次外层电子数2倍的元素 | |
| B. | 原子M层电子数等于L层和K层电子数之差的元素 | |
| C. | 第三周期ⅦA族的元素 | |
| D. | 最高正价和最低负价的绝对值之差为2的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
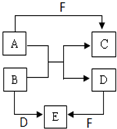 由短周期元素组成的中学常见的物质A、B、C、D、E、F的转化关系如图所示(部分反应条件略去):
由短周期元素组成的中学常见的物质A、B、C、D、E、F的转化关系如图所示(部分反应条件略去):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com