
| n |
| V |
| m |
| M |
| 6g |
| 60g/mol |
| n |
| V |
| 0.1mol |
| 0.1L |
| xmol/L |
| 10 |
| cV |
| 2 |
| cV |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 0.01 | 0.02 | 0.008 | 5 | |
| 2 | 800 | 0.02 | 0.03 | 0.017 | 1.6 | 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
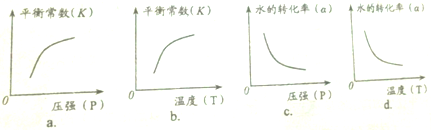
 ���㷺������ʳ���ɣ�ء����������ѣ��У������ܾ��п����ԣ��ܹ���1mol�û�������Ӧ��Br2��H2����������ֱ��ǣ�������
���㷺������ʳ���ɣ�ء����������ѣ��У������ܾ��п����ԣ��ܹ���1mol�û�������Ӧ��Br2��H2����������ֱ��ǣ�������| A��1mol��1mol |
| B��3.5mol��7mol |
| C��5mol��7mol |
| D��6mol��7mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
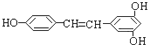
 ��1����֪��C��s��+O2��g��=CO2��g����H1=-393.5kJ/mol
��1����֪��C��s��+O2��g��=CO2��g����H1=-393.5kJ/mol�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������ƽ��ȡ11.7 g CuO��ĩ |
| B���ù㷺��pH��ֽ�����Һ��pHΪ6.2 |
| C���¶ȼ���ʾ�����¶���Ϊ25.69�� |
| D����100 mL��Ͳ��ȡ5.6 mL��ϡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
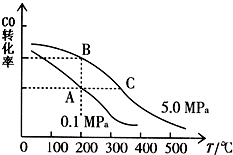
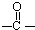 ���ṹ�����ʿɷ������з�Ӧ��
���ṹ�����ʿɷ������з�Ӧ��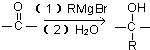
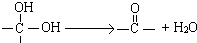
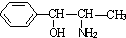 ����Ϊͬ���칹��
����Ϊͬ���칹��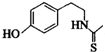 ������һ��������Ҳ�ܷ������Ƣ��Ļ�����Ӧ��д���û������������Ӧ�Ļ�ѧ����ʽ
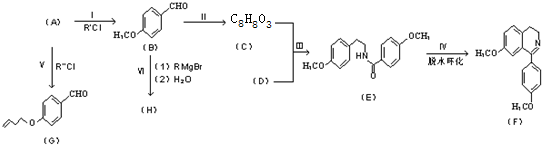
������һ��������Ҳ�ܷ������Ƣ��Ļ�����Ӧ��д���û������������Ӧ�Ļ�ѧ����ʽ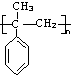 �ĺϳ�·������ͼ��
�ĺϳ�·������ͼ��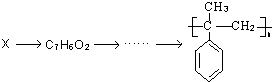
| HBr |
| N2OH��Һ |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
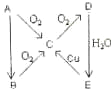 A��B��C��D��E����һ�������µ�ת��������ͼ��ʾ��
A��B��C��D��E����һ�������µ�ת��������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH3COONa |
| B��CuSO4 |
| C��NaOH |
| D��Na2CO3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com