
����Ŀ��������Ԫ��W��X ��Y ��Z �����ڱ��е����λ�������ʾ��������Ԫ��ԭ�ӵ�����������֮��Ϊ21 ���ش��������⣺
W | X | |||
Y | Z |
��1��X ��Ԫ�����ڱ��е�λ��Ϊ_______��
��2������Ԫ�ؼ����ӵİ뾶�ɴ�СΪ_____________�������ӷ��ű����
��3��W������⻯��ĵ���ʽΪ________________��
��4��W��Z ����������ˮ�������Խ�ǿ��Ϊ___________���ѧʽ����
��5��Y������Fe2O3 ��Ӧ�ܷų��������ȣ������ں��Ӹֹ죬�÷�Ӧ��ѧ����ʽΪ____________________��
��6����ʢ��3 mL ��������Һ���Թ�����뼸��W������������ˮ����Ũ��Һ��ʵ������Ϊ________________________________________��
��7��C3H7Z �Ľṹ��ʽ��____________________��
��8��ZX2������һ�ֹ���ɱ������������ҵ�Ͽ�����NaZX3��NaZ �������������Ƶ�ZX2 ͬʱ�õ�ZԪ�صĵ��ʣ��÷�Ӧ�����ӷ���ʽΪ_____________��
���𰸡� ��2���� ��A�壨��ڶ����� ��A�壩 Cl�D��N3�D��O2�D��Al3�� ![]() HClO4 2Al �� Fe2O3
HClO4 2Al �� Fe2O3 ![]() 2Fe �� Al2O3 ������ɫ����(��ɫ��������) CH3CH2CH2Cl��CH3CHClCH3 2ClO3�D �� 2Cl�D �� 4H�� �� 2ClO2�� �� Cl2�� �� 2H2O
2Fe �� Al2O3 ������ɫ����(��ɫ��������) CH3CH2CH2Cl��CH3CHClCH3 2ClO3�D �� 2Cl�D �� 4H�� �� 2ClO2�� �� Cl2�� �� 2H2O
����������ͼ����֪������Ԫ��ԭ�ӵ�����������֮��Ϊ21��Y������������Ϊx ������x+x+2+x+3+x+4=21�����x=3��WΪNԪ�ء�XΪOԪ�ء�YΪAlԪ�ء�ZΪClԪ������1��X Ϊ��Ԫ�أ���Ԫ�����ڱ��е�λ��Ϊ��2���� ��A���ڶ����� ��A�壻��2������Ԫ�ؼ����ӳ������Ӷ�һ�����Ӳ㣬�뾶����������Ӿ�����ͬ�ĵ��Ӳ�ṹ���˵����Խ�뾶ԽС����뾶�ɴ�СΪCl�D��N3�D��O2�D��Al3������3��WΪ��Ԫ�أ�������⻯��NH3�ĵ���ʽΪ![]() ����4�������ȵ�����������ˮ����HNO3��HClO4���Խ�ǿ��ΪHClO4����5����������Fe2O3 ��Ӧ�ܷų��������ȣ������ں��Ӹֹ죬�÷�Ӧ��ѧ����ʽΪ2Al �� Fe2O3
����4�������ȵ�����������ˮ����HNO3��HClO4���Խ�ǿ��ΪHClO4����5����������Fe2O3 ��Ӧ�ܷų��������ȣ������ں��Ӹֹ죬�÷�Ӧ��ѧ����ʽΪ2Al �� Fe2O3 ![]() 2Fe �� Al2O3����6����ʢ��3 mL ��������Һ���Թ�����뼸��W������������ˮ����HNO3Ũ��Һ��������ɫ��Ӧ��ʵ������Ϊ������ɫ������ɫ�������ƣ���7��C3H7Z ΪC3H7Cl����ṹ��ʽ��CH3CH2CH2Cl��CH3CHClCH3����8��ClO2������һ�ֹ���ɱ������������ҵ�Ͽ�����NaClO3��NaCl�������������Ƶ�ClO2ͬʱ�õ��������÷�Ӧ�����ӷ���ʽΪ2ClO3�D �� 2Cl�D �� 4H�� �� 2ClO2�� �� Cl2�� �� 2H2O��
2Fe �� Al2O3����6����ʢ��3 mL ��������Һ���Թ�����뼸��W������������ˮ����HNO3Ũ��Һ��������ɫ��Ӧ��ʵ������Ϊ������ɫ������ɫ�������ƣ���7��C3H7Z ΪC3H7Cl����ṹ��ʽ��CH3CH2CH2Cl��CH3CHClCH3����8��ClO2������һ�ֹ���ɱ������������ҵ�Ͽ�����NaClO3��NaCl�������������Ƶ�ClO2ͬʱ�õ��������÷�Ӧ�����ӷ���ʽΪ2ClO3�D �� 2Cl�D �� 4H�� �� 2ClO2�� �� Cl2�� �� 2H2O��


 �Ǽ�����������ϵ�д�
�Ǽ�����������ϵ�д� â���̸������Ծ�ϵ�д�
â���̸������Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz�����Һ��H2C2O4��HC2O4-��C2O42-�������ķֲ�������ij�����ʵ���Ũ�������������ʵ���Ũ�Ⱥ͵ı�ֵ����pH�Ĺ�ϵ�������й�˵������ȷ����

A. pH=5 ����Һ��c(C2O42-)>c(HC2O4-)
B. NaHC2O4��Һ�У�c(OH-)+c(C2O42-)=c(H+)+c(H2C2O4)
C. ��NaHC2O4��Һ�м�ǿ����pH��a���Ӧʱ����Һ�� 2c(Na+)=c(HC2O4-)+ c(H2C2O4)
D. Ϊʹ��Һ��c(c(HC2O4-)�����ܶ�һЩ����Һ��pH��ÿ�����2.7����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ѷ����Ԫ������MnCO3�ڿ����м�����ת��Ϊ��ͬ��̬�̵�������������������¶ȱ仯����ͼ������˵������ȷ���ǣ� ��
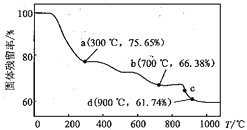
A. a ��ʣ�������n(Mn) : n(O) = 1 : 2
B. b ���Ӧ����ijɷ�ΪMn3O4
C. c �㷢���ķ�ӦΪ2MnO2 �� 2MnO+O2��
D. d ���Ӧ����ijɷ�ΪMnO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ҫ��������л�ѧ����ʽ����������ʽ��
��1����ҵ�õ�ⱥ��ʳ��ˮ�������Ļ�ѧ����ʽΪ____________________��
��2�������Ƶ�Na2S ��Һ�еμ����Ƶ���ˮ����������ʽΪ_______________��
��3���Ȼ��������NaOH ��Һ��Ӧ����������ʽΪ____________________��
��4���Ҵ�����������ȩ�Ļ�ѧ����ʽΪ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в�����Ӱ��ⶨ1mol���������ʵ��������
A.������©��
B.þ��������,��ɰƤ��ȥ����������
C.�����Թ���
D.��ȡҺ����ƿ�����������Ϊ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ�Ĺ�ҵԭ�ϡ���ҵ���������з�Ӧ����������ܵ��Ƿ�©����3Cl2+8NH3=N2+6NH4Cl������˵���������
A. ���а��̲�����ܵ�©�� B. �÷�Ӧ��NH4Cl�ǻ�ԭ����
C. ��Ӧ��NH3ֻ�Ի�ԭ�� D. ����1.4gN2ʱת��0.3mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽��Na ��CO2��Ӧ���ij��ѧ��ȤС�鰴��ͼװ�ý���ʵ�顣
��֪��CO + 2Ag ( NH3) 2OH=2Ag��+( NH4 ) 2CO3 +2NH3

�ش��������⣺
��1��д��A �з�Ӧ�����ӷ���ʽ__________________________��
��2������X ��������_____________��B �е���ҺΪ________________��
��3���ȳ���Ӳ�ʲ����ܵ�����Ϊm1 g ������Ʒװ��Ӳ�ʲ������У��Ƶ���Ʒ��Ӳ�ʲ����ܵ���������m2 g ���ٽ�������ʵ�����������ȷ˳����________�����ţ���
a����ȼ�ƾ��ƣ����� b��Ϩ��ƾ��� c���ر�K1��K2
d����K1��K2��ͨ��CO2��E �г��ֻ���
e������Ӳ�ʲ����� f����ȴ������
�ظ������������裬ֱ��Ӳ�ʲ����ܺ��أ��Ƶ�����Ϊm3 g ��
��4������Ӳ�ʲ�����һ��ʱ�䣬�۲쵽��������
�� �ƿ�����ڣ����ڳɽ���С��
�� �������ȣ���Ѹ��ȼ�գ�������ɫ���档��Ӧ��ȫ�����д�����ɫ���ʣ��� F ���Թ��ڱ����������ʲ�����
���������������ԭ����____________________________________��
��5��̽�����������Ԫ��Na �Ĵ�����ʽ
����һ��ֻ��Na2CO3���������ֻ��Na2O ����������Na2O��Na2CO3����
�������ʵ����ƣ���֤�������裺
���� | ���� | ���� |
1 | ��Ӳ�ʲ������еĹ����������ˮ����� | ����һ���� |
2 | ������1������Һ��___________________________ | |
3 | _____________________________________________ |
��6����������ʵ�������±�ʵ�����ݣ�д��Na ��CO2��Ӧ���ܻ�ѧ����ʽ___________��
m1 | m2 | m3 |
66.7g | 69.0g | 72.1g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ҫ�Ļ���ԭ�ϣ���������ˮâ��(Na2SO4)��̿�ۻ�ԭ���Ʊ���ԭ��Ϊ��Na2SO4��2CNa2S��2CO2��������Ҫ�������£�

(1) ���������в���ϡ��Һ������ˮ���ã�������________________________________________________________________________��
(2) ��֪��I2��2S2O32��===2I����S4O62�������Ƶõ�Na2S��9H2O�����к���Na2S2O3��5H2O�����ʡ�Ϊ�ⶨ��Ʒ�ijɷ֣���������ʵ�飬�������£�
a. ȡ����10.00 g���500.00 mL��Һ��
b. ȡ������Һ25.00 mL�ڵ���ƿ�У��������ZnCO3����Һ��ȥNa2S���ˣ�����Һ�е���2��3�ε�����Һ����0.050 00 mol��L��1 I2��Һ�ζ����յ㣬��ȥ5.00 mL I2��Һ��
c. ��ȡ������Һ25.00 mL�ڵ���ƿ�У�����50.00 mL 0.050 00 mol��L��1��I2��Һ��������2��3�ε�����Һ�����ñ�Na2S2O3��Һ�ζ������I2����ȥ15.00 mL 0.100 0 mol��L��1 Na2S2O3��Һ��
������b����ZnCO3��ȥNa2S�����ӷ���ʽΪ____________��
���жϲ���c�еζ��յ�ķ���Ϊ______________��
������������Na2S��9H2O��Na2S2O3��5H2O��������������������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����Թ�ҵ�����е�CrԪ�ػ����������õĹ������£���֪�����ȡҺ�еĽ���������Ҫ��Cr3+�������������Fe2+��Fe3+��Al3+��Ca2+��Mg2+)��
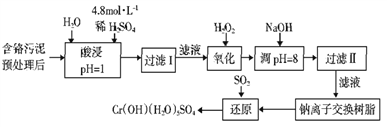
���������ӳ�����������������ʽ����ʱ��Һ��pH���±�:
������ | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
��ʼ����ʱ��pH | 1.9 | 7.0 | ���� | ���� | ���� |
������ȫʱ��pH | 3.2 | 9.0 | 11.1 | 8 | 9��>9�ܽ⣩ |
��1��ʵ������98%���ܶ�Ϊ1.84g��cm-3)��Ũ��������200 mL 4.8 mol��L-1��������Һ������ʱ��Ҫ��ȡ98%��Ũ��������Ϊ_______ mL������С�����һλС���������õIJ����������ձ�������������Ͳ����ʽ�ζ����⣬����_______��
��2�����˲���ʱ����Ҫ�Գ�������ϴ�ӣ�ϴ�ӳ����ķ�����_______��
��3������H2O2������һ����������+3��Crʹ֮ת���+6��Cr��CrO42-��Cr2O72-�����Ա������������ӷ��룺��һ������_______�������ӷ���ʽ��ʾ��
��4��������Һ��pH=8��ȥ������������_______��
��5�������ӽ�����֬��ԭ��Ϊ��Mn++nNaR��MRn+nNa+��������������������_______��
��6��ͨSO2����ʱ����ԭ���̷������·�Ӧ����дȱ�����ʲ���ƽ����
____ Na2Cr2O7+ SO2+ = Cr(OH)(H2O)5SO4+ Na2SO4��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com