
| A. | 橡皮擦--橡胶工业 | B. | 铝合金片--冶金工业 | ||
| C. | 铅笔芯--电镀工业 | D. | 铅笔漆--涂料工业 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
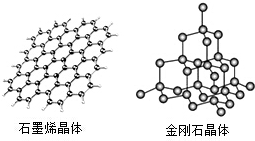 碳及其化合物广泛存在于自然界中,回答下列问题:
碳及其化合物广泛存在于自然界中,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
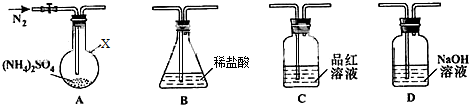
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3a+b-c | B. | c-3a-b | C. | a+b-c | D. | c-a-b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
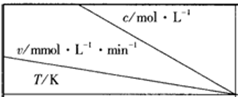 | 0.600 | 0.500 | 0.400 | 0.300 |
| 318.2 | 3.60 | 3.00 | 2.40 | 1.80 |
| 328.2 | 9.00 | 7.50 | a | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
| A. | a=6.00 | |
| B. | 同时改变反应温度和蔗糖的浓度,v可能不变 | |
| C. | b<318.2 | |
| D. | 不同温度时,蔗糖浓度减少一半所需的时间相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
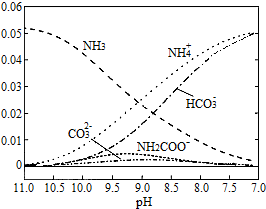
| A. | 在pH=9.0时,c(NH4+)>c(HCO3-)>c(NH2COO-)>c(CO32-) | |
| B. | 不同pH的溶液中存在关系:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-) | |
| C. | 随着CO2的通入,$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$不断增大 | |
| D. | 在溶液pH不断降低的过程中,有含NH2COO-的中间产物生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
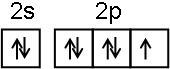 ;NF3中心原子轨道的杂化类型为sp3.
;NF3中心原子轨道的杂化类型为sp3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制0.1mol•L-1莫尔盐溶液500mL,需莫尔盐19.6克 | |
| B. | 可与含Fe2+、HClO、H+、Cl-微粒的溶液大量共存 | |
| C. | 加入过量Ba(OH)2溶液发生反应:2Ba2++2SO42-+Fe2++2OH-=2BaSO4↓+Fe(OH)2↓ | |
| D. | 取样,加入浓NaOH溶液并加热,出现可让蓝色石蕊试纸变红的气体,证明含NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com