
��13�֣���2L�ܱ������У�800��ʱ��Ӧ2NO(g)+O2(g)2NO2(g)��ϵ�У�
n(NO) ��ʱ��ı仯���±���
| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1��д���÷�Ӧ��ƽ�ⳣ������ʽ����=������ ������
��֪������300�棩������350�棩���÷�Ӧ�������� ������Ӧ������ȡ������ȡ�����
��2����ͼ�б�ʾNO2�ı仯�������������� ��������O2��Ũ�ȱ仯��ʾ��
0��2s�ڸ÷�Ӧ��ƽ�����ʦ�=����������������������
��3����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����________________
a�� �ԣ�NO2����2�ԣ�O2�� b��������ѹǿ���ֲ���
c�����棨NO��=2������O2�� d�����������ʵ��ܶȱ��ֲ���
��4����ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����___________
a����ʱ�����NO2���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч�Ĵ���
��5���������������С��1L����Ӧ�ﵽƽ��ʱ��ƽ�ⳣ�� �����������С�����䡱����
 �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �й����ʵ����ʵ���/mol | n��NO�� | n��H2O�� |
| �¶�T1 | 1.6 | 2.4 |
| �¶�T2 | 1.2 | 1.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 2C��g������10���ڷ�Ӧ��A��Ũ����1mol/L����0.6mol/L������CŨ�ȵı仯��ʾ�ĸ÷�Ӧ�����ʱ���ڵ�ƽ����Ӧ����Ϊ
2C��g������10���ڷ�Ӧ��A��Ũ����1mol/L����0.6mol/L������CŨ�ȵı仯��ʾ�ĸ÷�Ӧ�����ʱ���ڵ�ƽ����Ӧ����Ϊ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| [O2][H2]2 |
| [H2O]2 |
| [O2][H2]2 |
| [H2O]2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| N2+3H2?2NH3 | ||||
| �¶� | 25�� | 200�� | 400�� | 600�� |
| ƽ�ⳣ��K | 5��108 | 650 | 0.507 | 0.01 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
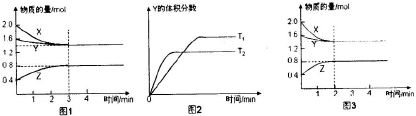
| A����Ӧ���е�ǰ3min�ڣ���X��ʾ�ķ�Ӧ����V��X��=0.1mol/��L?min�� | B��ƽ��ʱ�����ڵ�ѹǿΪ��Ӧǰ��0.8�� | C�����������������䣬�����¶ȣ���Ӧ�Ļ�ѧƽ�ⳣ��K��С | D�����ı䷴Ӧ������ʹ��Ӧ������ͼ3��ʾ����ı������������ѹǿ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com