
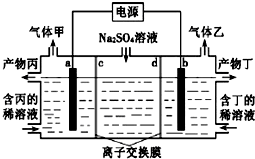
 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )| A. | a极与电源的正极相连 | |
| B. | 产物丙为硫酸溶液 | |
| C. | 离子交换膜d为阳离子交换膜(允许阳离子通过) | |
| D. | a电极反应式为2H2O+2e-═2OH-+H2↑ |
分析 电解硫酸钠溶液时,阳极上OH-放电生成O2、阴极上H+放电生成H2,所以实质上是电解H2O,同温同压下,转移电子相等时生成H2、O2的体积之比为2:1,同温同压下,气体甲与气体乙的体积比约为1:2,则甲是O2、乙是H2,所以a是阳极、b是阴极;
阳极附近有H+生成,所以产物丙是H2SO4,阴极附近有OH-生成,所以产物丁是NaOH,据此分析解答.
解答 解:电解硫酸钠溶液时,阳极上OH-放电生成O2、阴极上H+放电生成H2,所以实质上是电解H2O,同温同压下,转移电子相等时生成H2、O2的体积之比为2:1,同温同压下,气体甲与气体乙的体积比约为1:2,则甲是O2、乙是H2,所以a是阳极、b是阴极;
阳极附近有H+生成,所以产物丙是H2SO4,阴极附近有OH-生成,所以产物丁是NaOH,
A.通过以上分析知,a是阳极,则a与电源正极相连,故A正确;
B.通过以上分析知,产物丙是硫酸,故B正确;
C.电解质溶液中阳离子向阴极移动、阴离子向阳极移动,所以离子交换膜d为阳离子交换膜(允许阳离子通过),故C正确;
D.a电极反应式为2H2O-4e-═4H++O2↑,b电极反应式为2H2O+2e-═2OH-+H2↑,故D错误;
故选D.
点评 本题考查电解原理,为高频考点,正确判断阴阳极是解本题关键,难点是电极反应式的书写,熟练掌握离子放电顺序,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO4、BaCl2、HNO3 | B. | KNO3、Na2CO3、CaCl2 | ||
| C. | MgSO4、NaOH、H2SO4 | D. | AgNO3、NaCl、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L 氮气所含的原子数目为NA | |
| B. | 在反应3SiO2+6C+2N2=Si3N4+6CO,生成1 mol Si3N4时共转移12 NA电子 | |
| C. | 1molNa2O2固体中含离子总数为4 NA | |
| D. | 25℃时pH=13的NaOH溶液中含有Na+的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| … | E | A | B | ||
| C | … | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.03 mol/L | B. | 0.04 mol/L | C. | 0.05 mol/L | D. | 0.06mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2通入FeI2溶液中,可存在反应3Cl2+6FeI2=2FeCl3+4FeI3 | |
| B. | 每1mol Co2O3在酸性溶液中被还原生成Co2+时转移2 mol e- | |
| C. | FeCl3溶液能使淀粉-KI试纸变蓝 | |
| D. | I2具有较弱的氧化性,不可以将Co2+氧化成Co2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Kw/c(H+)=1 mol•L-1的溶液中:Na+、SiO32-、I-、CO32- | |
| B. | 氨水中:Al3+、K+、F-、NO3- | |
| C. | pH=1的溶液中:NH4+、Na+、SO42-、CH3COO- | |
| D. | 0.1 mol•L-1的NaHSO4溶液中:K+、Fe2+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com