
| A. | X单质可以把Y从其氢化物中置换出来 | |
| B. | X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 | |
| C. | 与H2化合时X单质比Y单质容易 | |
| D. | X原子的最外层电子数比Y原子的最外层电子数多 |
分析 比较非金属元素的非金属性强弱,可根据非金属单质之间的置换反应、与氢气化合的难易程度、对应最高价氧化物的水化物的酸性、氢化物的稳定性等角度判断.
解答 解:A.非金属元素的非金属性越强,其单质的氧化性越强,X单质可以把Y从其氢化物中置换出来,说明X的非金属性大于Y,故A不选;
B.元素的非金属性越强,其对应的最高价氧化物的水化物酸性越强,X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强,说明X的非金属性大于Y,故B不选;
C.与氢气越容易反应,则该非金属元素的非金属性越强,与H2化合时X单质比Y单质容易,说明X的非金属性大于Y,故C不选;
D.非金属性强弱与元素最外层电子数多少无关,如S元素非金属性N元素,故D选;
故选D.
点评 本题考查了非金属元素非金属性强弱的判断,根据元素周期律来分析解答即可,注意不能根据等电子多少判断非金属性强弱,要根据得电子难易程度判断,为易错点.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 等体积等浓度的HA和HB两种酸分别与足量的锌反应,用排水法收集气体 | HA放出氢气的反应速率更快 | 酸性:HB<HA |
| B | 以铜、铁、浓硝酸构成原电池 | 铁表面有红棕色气泡产生 | 铜作原电池的负极 |
| C | 向25mL冷水和沸水中分别滴入5滴FeCls饱和溶液 | 前者为黄色,后者为红褐色 | 升高温度,Fe3+的水解程度增大 |
| D | 将固体CaSO4加入Na2CO3饱和溶液中 | 一段时间后,检验固体主要成分为CaCO3 | Ksp ( CaSO4)<Ksp ( CaCO3 ) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 | |
| B. | 元素周期表共七个横行代表七个周期,18 个纵横代表18 个族 | |
| C. | 主、副族元素的族序数从左到右都是依次由小到大排列(如ⅠB→→ⅦB) | |
| D. | 除零族外,由长、短周期元素共同组成的元素族称为主族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
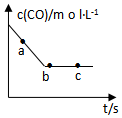 汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气:
汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气: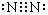 .
.| 实验编号 | 实验目的 | T/℃ | NO初始浓度 mol/L | CO初始浓度 mol/L | 同种催化剂的比表面积 m2/g | 达平衡时所用的时间min |
| Ⅰ | 参照实验 | 280 | 6.50×10-3 | 4.00×10-3 | 80 | t |
| Ⅱ | 280 | 6.50×10-3 | 4.00×10-3 | 120 | 0.5t | |
| Ⅲ | 360 | 6.50×10-3 | 4.00×10-3 | 80 | 0.2t |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
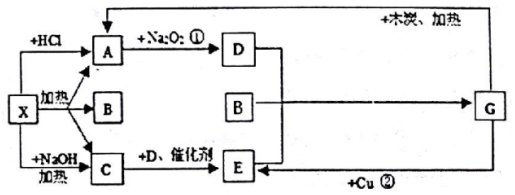
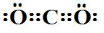 ;G的化学式为HNO3.
;G的化学式为HNO3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=13的溶液:K+、AlO2-、Cl-、S2- | |
| B. | 含有大量CO32-的溶液:Na+、Ca2+、Cl-、OH- | |
| C. | 含有大量SCN -的溶液:Na+、NH4+、Fe3+、Cl- | |
| D. | 水电离产生的c(H+)水=10-12mol•L-1的溶液:K+、Na+、Ca2+、ClO- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com