
���� ��1������װ���Ƿ�����Һ�����ʵ�鷽�������װ��ѡ����������
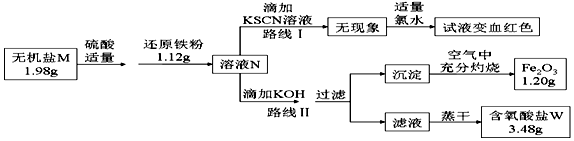
��2��Fe2O3��Al2O3��SiO2�Ļ����μӹ��������ַ�Ӧ����ˣ������������������Ȼ����������������������Ȼ������������費�����ᣬ��Ԫ��Ϊ�����Ӽ����Լ���KSCN��Һ��������ӱ��ɫ��
��3������Һ�еμӹ�������������Һ��ַ�Ӧ����ˣ������ķ�ӦΪ�������������������Һ��Ӧ�����Ȼ��ƺ�ˮ���������ӷ�Ӧ���������������������ӷ�Ӧ�������ǻ��������ƣ��ݴ���д���ӷ���ʽ��
��4��ϴ�Ӣ����ó�������ɺ���أ�����ΪB gΪ���������������Ԫ���غ������Ԫ�ص�����������
��� �⣺��1������װ���Ƿ�����Һ�����ʵ�鷽�������װ��ѡ��������Ϊ��ͨ©�������������ձ���
�ʴ�Ϊ����ͨ©�������������ձ���
��2��Fe2O3��Al2O3��SiO2�Ļ����μӹ��������ַ�Ӧ����ˣ������������������Ȼ����������������������Ȼ������������費�����ᣬ��Ԫ��Ϊ�����Ӽ����Լ���KSCN��Һ��������ӱ��ɫ�������������Һ����Ԫ�صĴ�����ʽ��Fe3+���������Ĵ����ǣ�ȡ������Һ���Թ��У��μ�һ��KSCN��Һ����Һ��죬
�ʴ�Ϊ��Fe3+��ȡ������Һ���Թ��У��μ�һ��KSCN��Һ����Һ��죻
��3������Һ�еμӹ�������������Һ��ַ�Ӧ����ˣ������ķ�ӦΪ���������������������Һ��Ӧ�����Ȼ��ƺ�ˮ����Ӧ�����ӷ���ʽΪ��H++OH-�TH2O���������ӷ�Ӧ����������������Ӧ�����ӷ���ʽΪ��Fe3++3OH-�TFe��OH��3�����������ӷ�Ӧ�������ǻ��������ƣ���Ӧ�����ӷ���ʽΪ��Al3++4OH-�T[Al��OH��4]-��
�ʴ�Ϊ��H++OH-�TH2O��Fe3++3OH-�TFe��OH��3����Al3++4OH-�T[Al��OH��4]-��
��4��ϴ�Ӣ����ó�������ɺ���أ�����ΪB gΪ���������������Ԫ���غ������Ԫ�ص���������=$\frac{\frac{Bg}{160g/mol}��2��56g/mol}{Ag}$��100%=$\frac{70B}{A}%$��
�ʴ�Ϊ��$\frac{70B}{A}%$��
���� ���⿼�������ʵķ�����������ӷ���ʽ����д�����ʺ����ļ���ȣ���Ŀ�����ڿ���ѧ�������������������ͼ�����������Ŀ�Ѷ��еȣ�


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д� �������ϵ�д�
�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ������Һ | B�� |  �к͵ζ� | ||
| C�� |  ��ȥ�屽���������嵥�� | D�� |  ��ȡ���ռ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Һ�е�SO42-������HCl�ữ��Ba��NO3��2��Һ���۲����ް�ɫ�������� | |
| B�� | ��ȥNO�л��е�����NO2�����������ͨ��ˮ�У������ſ������ռ�NO | |
| C�� | ��NaNO3������Ũ��������HNO3 | |
| D�� | ͨ��CO2�Գ�ȥNa2CO3��Һ�л��е�NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ClO2�����������ˮ�У�ClO2��Ũ��Ӧ��0.10��0.80mg/L֮�䣮�õ��������ˮ��C1O2Ũ�ȵ�ʵ�鲽�����£�
��ClO2�����������ˮ�У�ClO2��Ũ��Ӧ��0.10��0.80mg/L֮�䣮�õ��������ˮ��C1O2Ũ�ȵ�ʵ�鲽�����£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 144.0gCuSO4 | B�� | 144.0gCuSO4•5H2O | ||
| C�� | 255.0gCuSO4•5H2O | D�� | 250.0gCuSO4•5H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʵ��������� | B�� | ԭ������ | C�� | �������� | D�� | �ܶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com